Yersinia pestis is de veroorzaker van de pest. Wat weten we over de veroorzaker van de pest?
Meer dan de helft van de bevolking van Europa werd in de Middeleeuwen (XIV eeuw) weggevaagd door een plaag die bekend staat als de Zwarte Dood. De gruwel van deze epidemieën bleef na enkele eeuwen in de herinnering van mensen en werd zelfs vastgelegd in de schilderijen van kunstenaars. Vervolgens bezocht de pest Europa herhaaldelijk en eiste mensenlevens op, zij het niet in zulke hoeveelheden.
Momenteel blijft de pest een ziekte. Jaarlijks raken ongeveer tweeduizend mensen besmet. Van hen de meeste overlijdt. De meeste gevallen van infectie worden waargenomen in de noordelijke regio's van China en Centraal-Aziatische landen. Volgens deskundigen zijn er vandaag de dag geen redenen of voorwaarden voor het ontstaan van de zwarte dood.
De veroorzaker van de pest werd in 1894 ontdekt. Bij het bestuderen van epidemieën van de ziekte ontwikkelden Russische wetenschappers principes voor de ontwikkeling van de ziekte, de diagnose en behandeling ervan, en er werd een anti-pestvaccin gecreëerd.
Symptomen van de pest zijn afhankelijk van de vorm van de ziekte. Wanneer de longen worden aangetast, worden patiënten zeer besmettelijk, omdat de infectie zich via druppeltjes in de lucht naar de omgeving verspreidt. Bij de builenvorm van de pest zijn patiënten enigszins besmettelijk of helemaal niet besmettelijk. Er zijn geen ziekteverwekkers in de afscheidingen van de aangetaste lymfeklieren, of er zijn er maar heel weinig.
De behandeling van de pest is veel effectiever geworden met de komst van moderne antibacteriële medicijnen. Het sterftecijfer als gevolg van de pest is sindsdien gedaald tot 70%.
Pestpreventie omvat een aantal maatregelen om de verspreiding van infecties te beperken.
De pest is een acute infectieuze zoönose door vectoren overgedragen ziekte, dat in de GOS-landen, samen met ziekten als cholera, tularemie en pokken, wordt beschouwd als (OOI).
Rijst. 1. Schilderij ‘De triomf van de dood’. Pieter Bruegel.
Pest agent
In 1878 ontdekten G. N. Minkh en in 1894 A. Yersin en S. Kitazato onafhankelijk van elkaar de veroorzaker van de pest. Vervolgens bestudeerden Russische wetenschappers het mechanisme van de ontwikkeling van de ziekte, de principes van diagnose en behandeling, en creëerden een anti-pestvaccin.
- De veroorzaker van de ziekte (Yersinia pestis) is een bipolaire, niet-beweeglijke coccobacillus, die een delicate capsule heeft en nooit sporen vormt. Het vermogen om een capsule en antifagocytisch slijm te vormen, zorgt ervoor dat macrofagen en leukocyten de ziekteverwekker niet actief kunnen bestrijden, waardoor het zich snel vermenigvuldigt in de organen en weefsels van mensen en dieren, zich verspreidt via de bloedbaan en via het lymfestelsel door het hele lichaam. lichaam.
- Pestpathogenen produceren exotoxinen en endotoxinen. Exo- en endotoxinen bevinden zich in de lichamen en capsules van bacteriën.
- Enzymen van bacteriële agressie (hyaluronidase, coagulase, fibrinolysine, hemolysine) vergemakkelijken hun penetratie in het lichaam. De stick kan zelfs de intacte huid binnendringen.
- In de grond verliest de pestbacil zijn levensvatbaarheid gedurende enkele maanden niet. Het overleeft maximaal een maand in de lijken van dieren en knaagdieren.
- Bacteriën zijn resistent tegen lage temperaturen en bevriezen.
- Pestpathogenen zijn gevoelig voor hoge temperaturen, een zure omgeving en zonnestralen, waardoor ze in slechts 2 - 3 uur worden gedood.
- Ziekteverwekkers worden maximaal 30 dagen in pus, maximaal 3 maanden in melk en maximaal 50 dagen in water bewaard.
- Desinfectiemiddelen vernietigen de pestbacil binnen enkele minuten.
- Pestpathogenen veroorzaken ziekten bij 250 diersoorten. Onder hen bestaat de meerderheid uit knaagdieren. Kamelen, vossen, katten en andere dieren zijn vatbaar voor de ziekte.

Rijst. 2. Op de foto is de pestbacil de bacterie die de pest veroorzaakt: Yersinia pestis.
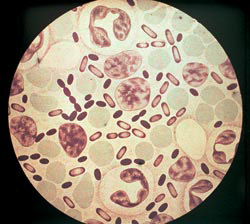
Rijst. 3. De foto toont de veroorzakers van de pest. De intensiteit van de kleuring bij anilinekleurstoffen is het grootst aan de polen van bacteriën.
Php?post=4145&action=edit#
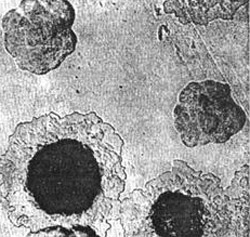
Rijst. 4. Op de foto groeien de ziekteverwekkers van de pest op een dicht koloniemedium. In eerste instantie lijken de kolonies op gebroken glas. Vervolgens wordt hun centrale deel dichter en lijkt de omtrek op kant.
Epidemiologie
Reservoir van infectie
Knaagdieren (tarbagans, marmotten, gerbils, gophers, ratten en huismuizen) en dieren (kamelen, katten, vossen, hazen, egels, enz.) zijn gemakkelijk vatbaar voor de pestbacil. Bij proefdieren zijn witte muizen vatbaar voor infecties, cavia's, konijnen en apen.
Honden krijgen nooit de pest, maar ze dragen de ziekteverwekker over via de beten van bloedzuigende insecten: vlooien. Een dier dat aan een ziekte sterft, is niet langer een bron van infectie. Als knaagdieren die besmet zijn met pestbacillen overwinteren, wordt hun ziekte latent en na de winterslaap worden ze opnieuw verspreiders van ziekteverwekkers. In totaal zijn er wel 250 diersoorten die ziek zijn en daarom een bron en reservoir van infecties zijn.

Rijst. 5. Knaagdieren zijn het reservoir en de bron van de pestziekte.

Rijst. 6. De foto vertoont tekenen van pest bij knaagdieren: vergrote lymfeklieren en meerdere bloedingen onder de huid.

Rijst. 7. Op de foto is de kleine jerboa drager van de pest in Centraal-Azië.

Rijst. 8. Op de foto is de zwarte rat niet alleen drager van de pest, maar ook van leptospirose, leishmaniasis, salmonellose, trichinose, enz.
Routes van infectie
- De belangrijkste overdrachtsroute van ziekteverwekkers is via vlooienbeten (overdraagbare route).
- De infectie kan het menselijk lichaam binnendringen bij het werken met zieke dieren: slachten, villen en snijden (contactroute).
- Ziekteverwekkers kunnen met besmette voedingsmiddelen het menselijk lichaam binnendringen als gevolg van onvoldoende warmtebehandeling.
- Van een patiënt met longvorm Pestinfectie wordt verspreid door druppeltjes in de lucht.

Rijst. 9. De foto toont een vlo op de menselijke huid.

Rijst. 10. De foto toont het moment van een vlooienbeet.
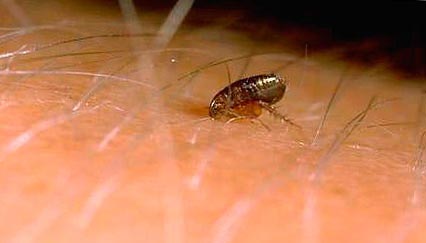
Rijst. 11. Het moment van een vlooienbeet.
Pathogeendragers
- De dragers van ziekteverwekkers zijn vlooien (in de natuur zijn er meer dan 100 soorten van deze geleedpotige insecten),
- Sommige soorten teken zijn dragers van ziekteverwekkers.
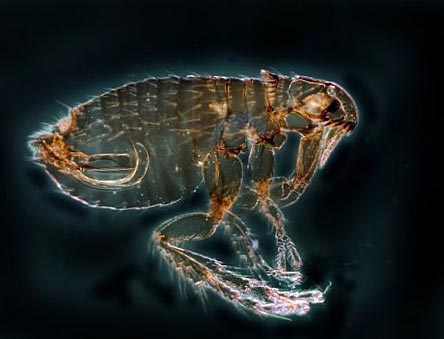
Rijst. 12. Op de foto is de vlo de belangrijkste drager van de pest. Er zijn meer dan 100 soorten van deze insecten in de natuur.

Rijst. 13. Op de foto is de gophervlo de belangrijkste drager van de pest.
Hoe ontstaat een infectie?
Infectie vindt plaats door een insectenbeet en het wrijven van de ontlasting en de darminhoud tijdens het oprispen tijdens het voeden. Wanneer bacteriën zich vermenigvuldigen in de darmbuis van een vlo onder invloed van coagulase (een enzym dat wordt uitgescheiden door ziekteverwekkers), wordt er een ‘plug’ gevormd die voorkomt dat menselijk bloed het lichaam binnendringt. Als gevolg hiervan braakt de vlo een stolsel uit op de huid van de gebeten persoon. Geïnfecteerde vlooien blijven 7 weken tot 1 jaar zeer infectieus.

Rijst. 14. Op de foto is het uiterlijk van een vlooienbeet pulicotische irritatie.
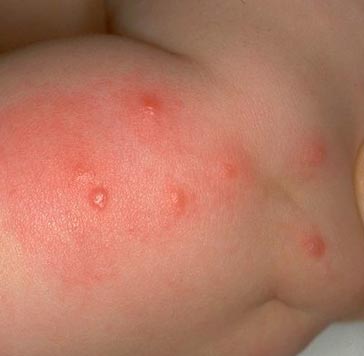
Rijst. 15. De foto toont een karakteristieke reeks vlooienbeten.

Rijst. 16. Aanzicht van het onderbeen met vlooienbeten.

Rijst. 17. Uiterlijk van de dij met vlooienbeten.
De mens als besmettingsbron
- Wanneer de longen worden aangetast, worden patiënten zeer besmettelijk. De infectie verspreidt zich via druppeltjes in de lucht naar het milieu.
- Bij de builenvorm van de pest zijn patiënten enigszins besmettelijk of helemaal niet besmettelijk. Er zijn geen ziekteverwekkers in de afscheidingen van de aangetaste lymfeklieren, of er zijn er maar heel weinig.
Mechanismen van de ontwikkeling van de pest
Het vermogen van de pestbacil om een capsule en antifagocytisch slijm te vormen, staat macrofagen en leukocyten niet toe om het actief te bestrijden, waardoor de ziekteverwekker zich snel vermenigvuldigt in de organen en weefsels van mens en dier.
- Pestpathogenen dringen door de beschadigde huid en vervolgens via het lymfestelsel naar de lymfeklieren, die ontstoken raken en conglomeraten (buboes) vormen. Ontsteking ontwikkelt zich op de plaats van de insectenbeet.
- Penetratie van de ziekteverwekker in de bloedbaan en de massale reproductie ervan leidt tot de ontwikkeling van bacteriële sepsis.
- Bij een patiënt met een longpest verspreidt de infectie zich via druppeltjes in de lucht. De bacteriën dringen de longblaasjes binnen en veroorzaken ernstige longontsteking.
- Als reactie op de enorme verspreiding van bacteriën produceert het lichaam van de patiënt een groot aantal ontstekingsmediatoren. Ontwikkelen gedissemineerd intravasculair coagulatiesyndroom(DIC-syndroom), waarbij iedereen last heeft interne organen. Bloedingen in de hartspier en de bijnieren vormen een bijzonder gevaar voor het lichaam. De ontwikkelde infectieuze-toxische shock veroorzaakt de dood van de patiënt.
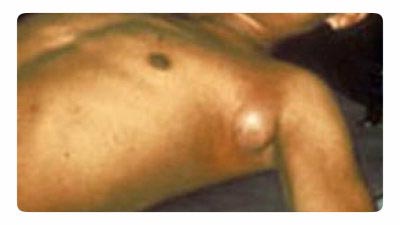
Rijst. 18. De foto toont de builenpest. Typische vergroting van de lymfeklier in het okselgebied.
Symptomen van de pest
De ziekte manifesteert zich nadat de ziekteverwekker het lichaam binnenkomt op dag 3-6 (zelden, maar er zijn gevallen geweest waarbij de ziekte zich op dag 9 manifesteerde). Wanneer de infectie in het bloed terechtkomt, bedraagt de incubatietijd enkele uren.
Klinisch beeld van de beginperiode
- Acuut begin, hoge temperaturen en koude rillingen.
- Myalgie (spierpijn).
- Ondraaglijke dorst.
- Een sterk teken van zwakte.
- Snelle ontwikkeling van psychomotorische agitatie (“dergelijke patiënten worden gek genoemd”). Op het gezicht verschijnt een masker van afschuw ("pestmasker"). Lethargie en apathie komen minder vaak voor.
- Het gezicht wordt hyperemisch en gezwollen.
- De tong is dik bedekt met een witte coating (“krijtachtige tong”).
- Er verschijnen meerdere bloedingen op de huid.
- De hartslag neemt aanzienlijk toe. Aritmie verschijnt. De bloeddruk daalt.
- De ademhaling wordt oppervlakkig en snel (tachypneu).
- De hoeveelheid uitgescheiden urine neemt sterk af. Er ontstaat anurie (volledige afwezigheid van urineproductie).
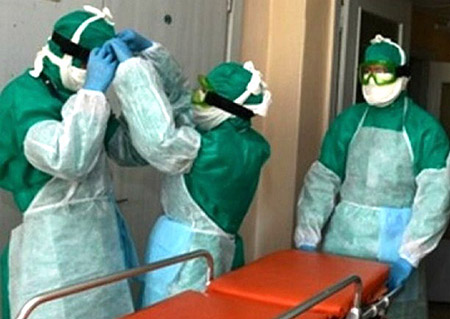
Rijst. 19. Op de foto wordt hulp aan een pestpatiënt verleend door artsen gekleed in antipestpakken.
Vormen van de pest
Lokale vormen van de ziekte
Cutane vorm
Op de plaats van een vlooienbeet of contact met een besmet dier huid er verschijnt een papule, die snel zweert. Vervolgens verschijnen er een zwarte korst en litteken. Meestal zijn huidmanifestaties de eerste tekenen van ernstigere manifestaties van de pest.
Builenvorm
De meest voorkomende vorm van manifestatie van de ziekte. Vergrote lymfeklieren verschijnen nabij de plaats van de insectenbeet (lies, axillair, cervicaal). Vaker raakt één lymfeklier ontstoken, minder vaak meerdere. Wanneer meerdere lymfeklieren tegelijk ontstoken raken, ontstaat er een pijnlijke bubo. Aanvankelijk heeft de lymfeklier een harde consistentie, pijnlijk bij palpatie. Geleidelijk wordt het zachter en krijgt het een deegachtige consistentie. Vervolgens verdwijnt de lymfeklier of wordt deze zwerend en scleroserend. Vanuit de aangetaste lymfeklier kan de infectie in de bloedbaan terechtkomen, met de daaropvolgende ontwikkeling van bacteriële sepsis. Acute fase De builenpestvorm duurt ongeveer een week.

Rijst. 20. De foto toont de aangetaste cervicale lymfeklieren (buboes). Meerdere bloedingen van de huid.
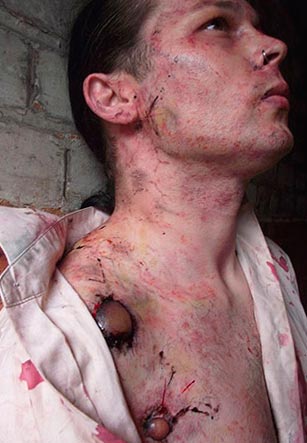
Rijst. 21. Op de foto is de builenpest een nederlaag cervicale lymfeklieren. Meerdere bloedingen in de huid.

Rijst. 22. De foto toont de builenvorm van de pest.
Gangbare (gegeneraliseerde) vormen
Wanneer de ziekteverwekker in de bloedbaan terechtkomt, ontwikkelen zich wijdverspreide (gegeneraliseerde) vormen van pest.
Primaire septische vorm
Als de infectie, waarbij de lymfeklieren worden omzeild, onmiddellijk in het bloed terechtkomt, ontwikkelt zich de primaire septische vorm van de ziekte. Intoxicatie ontwikkelt zich razendsnel. Met de enorme proliferatie van ziekteverwekkers in het lichaam van de patiënt wordt een groot aantal ontstekingsmediatoren geproduceerd. Dit leidt tot de ontwikkeling van het gedissemineerde intravasculaire coagulatiesyndroom (DIC), dat alle inwendige organen aantast. Bloedingen in de hartspier en de bijnieren vormen een bijzonder gevaar voor het lichaam. De ontwikkelde infectieuze-toxische shock veroorzaakt de dood van de patiënt.
Secundaire septische vorm van de ziekte
Wanneer de infectie zich buiten de aangetaste lymfeklieren verspreidt en ziekteverwekkers in de bloedbaan terechtkomen, ontstaat infectieuze sepsis, die zich manifesteert scherpe verslechtering de toestand van de patiënt, verhoogde symptomen van intoxicatie en de ontwikkeling van het DIC-syndroom. De ontwikkelde infectieuze-toxische shock veroorzaakt de dood van de patiënt.

Rijst. 23. Op de foto is de septische vorm van de pest het gevolg van het gedissemineerde intravasculaire coagulatiesyndroom.

Rijst. 24. Op de foto is de septische vorm van de pest het gevolg van het gedissemineerde intravasculaire coagulatiesyndroom.
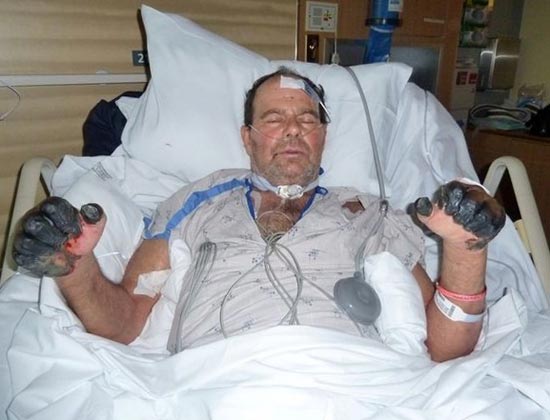
Rijst. 25. 59-jarige Paul Gaylord (inwoner van Portland, Oregon, VS). Pestbacteriën kwamen zijn lichaam binnen via een zwerfkat. Als gevolg van de ontwikkeling van een secundaire septische vorm van de ziekte werden zijn vingers en tenen geamputeerd.

Rijst. 26. Gevolgen van het DIC-syndroom.
Extern verspreide vormen van de ziekte
Primaire longvorm
De pneumonische vorm van de pest is de ernstigste en gevaarlijkste vorm van de ziekte. De infectie dringt de longblaasjes binnen via druppeltjes in de lucht. Schade aan het longweefsel gaat gepaard met hoesten en kortademigheid. Er treedt een stijging van de lichaamstemperatuur op ernstige koude rillingen. Het sputum aan het begin van de ziekte is dik en transparant (glasvocht), daarna wordt het vloeibaar en schuimig, vermengd met bloed. De schaarse gegevens uit lichamelijk onderzoek komen niet overeen met de ernst van de ziekte. DIC-syndroom ontwikkelt zich. Interne organen worden aangetast. Bloedingen in de hartspier en de bijnieren vormen een bijzonder gevaar voor het lichaam. De dood van de patiënt vindt plaats als gevolg van een infectieuze-toxische shock.
Wanneer de longen worden aangetast, worden patiënten zeer besmettelijk. Ze vormen rondom zichzelf een brandpunt van een bijzonder gevaarlijke infectieziekte.
Secundaire longvorm
Het is een uiterst gevaarlijke en ernstige vorm van de ziekte. Ziekteverwekkers dringen het longweefsel binnen vanuit de aangetaste lymfeklieren of via de bloedbaan tijdens bacteriële sepsis. Het klinische beeld en de uitkomst van de ziekte zijn hetzelfde als bij de primaire longvorm.
Intestinale vorm
Het bestaan van deze vorm van de ziekte wordt als controversieel beschouwd. Aangenomen wordt dat besmetting plaatsvindt door de consumptie van besmette producten. Aanvankelijk verschijnen tegen de achtergrond van het intoxicatiesyndroom buikpijn en braken. Dan komt diarree en talrijke driften (tenesmus). De ontlasting is overvloedig, slijmerig en bloederig.
Rijst. 27. Foto van een anti-pestpak - speciale uitrusting voor medisch personeel bij het elimineren van een uitbraak van een bijzonder gevaarlijke infectieziekte.
Laboratoriumdiagnose van de pest
De basis voor het diagnosticeren van de pest is de snelle detectie van de pestbacil. Eerst wordt bacterioscopie van uitstrijkjes uitgevoerd. Vervolgens wordt een kweek van de ziekteverwekker geïsoleerd, die proefdieren infecteert.
Het materiaal voor onderzoek is de inhoud van de bubo, sputum, bloed, ontlasting, stukjes weefsel van organen van overleden dieren en lijken.
Bacterioscopie
De veroorzaker van de pest (Yersinia pestis) is een staafvormige bipolaire coccobacilli. Analyse voor de detectie van pestbacillen door directe bacterioscopie is het eenvoudigst op een snelle manier. De wachttijd voor de uitslag bedraagt maximaal 2 uur.
Gewassen van biologisch materiaal
De cultuur van de pestziekte wordt geïsoleerd in gespecialiseerde, zwaarbeveiligde laboratoria die zijn ontworpen om mee te werken. De groeitijd van de pathogenencultuur is twee dagen. Vervolgens wordt een antibioticagevoeligheidstest uitgevoerd.
Serologische methoden
Het gebruik van serologische methoden maakt het mogelijk om de aanwezigheid en groei van antilichamen in het bloedserum van de patiënt tegen de pestpathogeen te bepalen. De tijd om resultaten te ontvangen is 7 dagen.

Rijst. 28. De diagnose van pest wordt uitgevoerd in speciale gevoelige laboratoria.

Rijst. 29. De foto toont de veroorzakers van de pest. Fluorescentiemicroscopie.

Rijst. 30. De foto toont de cultuur van Yersinia pestis.
Immuniteit tegen de pest
Antilichamen tegen de introductie van de pestziekte worden tijdig gevormd late data ontwikkeling van de ziekte. De immuniteit na een ziekte is niet langdurig of intens. Er zijn herhaalde gevallen van de ziekte, die net zo ernstig zijn als de eerste.
Behandeling van de pest
Voordat de behandeling begint, wordt de patiënt in een aparte kamer in het ziekenhuis opgenomen. Medische staf, die de patiënt bedient, kleedt zich in een speciaal anti-pestpak.
Antibacteriële behandeling
Antibacteriële behandeling begint bij de eerste tekenen en manifestaties van de ziekte. Onder antibiotica wordt de voorkeur gegeven antibacteriële medicijnen aminoglycosidegroep (streptomycine), tetracyclinegroep (vibromycine, morfocycline), fluorochinolongroep (ciprofloxacine), ansamycinegroep (rifampicine). Een antibioticum uit de amfenicolgroep (cortrimoxazol) heeft zichzelf goed bewezen bij de behandeling van de huidvorm van de ziekte. Voor septische vormen van de ziekte wordt een combinatie van antibiotica aanbevolen. Het verloop van de antibacteriële therapie bedraagt minimaal 7-10 dagen.
Behandeling gericht op verschillende stadia van ontwikkeling van het pathologische proces
Het doel van pathogenetische therapie is het verminderen van het intoxicatiesyndroom door gifstoffen uit het bloed van de patiënt te verwijderen.
- De toediening van vers ingevroren plasma, eiwitgeneesmiddelen, reopolyglucine en andere geneesmiddelen in combinatie met geforceerde diurese is geïndiceerd.
- Verbeterde microcirculatie wordt bereikt door trental te gebruiken in combinatie met salcoseryl of picamilon.
- Als zich bloedingen voordoen, wordt onmiddellijk plasmaferese uitgevoerd om het gedissemineerde intravasculaire coagulatiesyndroom te verlichten.
- Als de bloeddruk daalt, wordt dopamide voorgeschreven. Deze aandoening duidt op de generalisatie en ontwikkeling van sepsis.
Symptomatische behandeling
Symptomatische behandeling is gericht op het onderdrukken en elimineren van de manifestaties (symptomen) van de pest en als resultaat het verlichten van het lijden van de patiënt. Het is gericht op het elimineren van pijn, hoesten, kortademigheid, verstikking, tachycardie, enz.
De patiënt wordt als gezond beschouwd als alle symptomen van de ziekte verdwenen zijn en 3 negatieve resultaten bacteriologisch onderzoek.
Anti-epidemische maatregelen
Identificatie van een pestpatiënt is een signaal voor onmiddellijke actie, waaronder:
- het uitvoeren van quarantainemaatregelen;
- onmiddellijke isolatie van de patiënt en het uitvoeren van preventieve maatregelen antibacteriële behandeling servicepersoneel;
- desinfectie bij de bron van de ziekte;
- vaccinatie van personen die in contact komen met de patiënt.
Na vaccinatie met een anti-pestvaccin duurt de immuniteit een jaar. Hervaccinatie na 6 maanden. personen die gevaar lopen herinfectie: herders, jagers, landarbeiders en medewerkers van anti-pestinstellingen.

Rijst. 31. Op de foto is het medische team gekleed in anti-pestpakken.
Ziekteprognose
De prognose van de pest hangt af van de volgende factoren:
- vormen van de ziekte,
- tijdigheid van de gestarte behandeling,
- beschikbaarheid van het gehele arsenaal aan medicinale en niet-medicamenteuze behandelingen.
De gunstigste prognose is voor patiënten met betrokkenheid van de lymfeklieren. Het sterftecijfer voor deze vorm van de ziekte bedraagt 5%. In de septische vorm van de ziekte bereikt het sterftecijfer 95%.
De pest verschijnt en zelfs met het gebruik van alles wat nodig is geneesmiddelen en manipulatie eindigt de ziekte vaak in de dood van de patiënt. Pestpathogenen circuleren voortdurend in de natuur en kunnen niet volledig worden vernietigd en gecontroleerd. De symptomen van de pest zijn gevarieerd en afhankelijk van de vorm van de ziekte. De builenpestvorm komt het meest voor.
Artikelen in de sectie "Bijzonder gevaarlijke infecties"Meest populair
Artikel voor de wedstrijd “bio/mol/tekst”: Op het eerste gezicht is het een microscopisch kleine en onschadelijke bacterie, maar in werkelijkheid is het een meedogenloze moordenaar die in de 14e eeuw bijna een derde van de Europese bevolking doodde. Yersinia pestis, in de volksmond bekend als pest stok, is de veroorzaker van de gevaarlijkste ziekte: de pest. Sinds de oudheid rond Y. pestis Er ontstonden wetenschappelijke geschillen die tot op de dag van vandaag voortduren. De meest opvallende daarvan, evenals feiten uit het leven van een van de meest mysterieuze micro-organismen, worden in dit artikel belicht.
Opmerking!
Dit werk behaalde de eerste plaats in de categorie “Beste Nieuwsbericht” van de wedstrijd “bio/mol/tekst” 2015.
De sponsor van de nominatie ‘Beste artikel over de mechanismen van veroudering en een lang leven’ is de Science for Life Extension Foundation. De publieksprijs werd gesponsord door Helicon.
Competitiesponsors: Biotechnology Research Laboratory 3D Bioprinting Solutions en Scientific Graphics, Animation and Modeling Studio Visual Science.
Vreemdeling in een masker
Y. pestis was vanwege vele omstandigheden lange tijd verborgen voor het menselijk oog. Aanvankelijk was de grootte een obstakel: vóór de uitvinding van de microscoop door de gebroeders Jansen in 1590* en het verdere gebruik ervan door Hooke en Leeuwenhoek (aan wie overigens bacteriën en protozoa werden geboren) dacht niemand zelfs maar aan de microscoop. feit dat er naast levende objecten die zichtbaar zijn voor het oog, ook kleine organismen bestaan. Maar zelfs met de komst van de optica bleef de peststaf zijn incognitostatus behouden, waarbij de bacteriën van de geboorte de schuld kregen. Bacterie, Bacil En Pasteurella. In de tussentijd Y. pestis liep vrij rond de wereld en werd meegesleept mensenlevens meer dan oorlog.
Er zijn door de geschiedenis heen drie bekende pestpandemieën geweest. De eerste hiervan was de “Justijnse Pest” (genoemd naar de Byzantijnse heerser Justinianus I), die de hele beschaafde wereld van die tijd overspoelde. Historici dateren het terug tot 541-580 na Christus, hoewel uitbraken van een onbekende ziekte de mensheid nog twee eeuwen lang teisterden. Volgens de beroemde vectoronderzoeker, medisch entomoloog Milan Daniel, stierven op het hoogtepunt van de ziekte in Constantinopel (nu Istanbul, Turkije) dagelijks tot tienduizend mensen. Op basis van modern onderzoek hebben wetenschappers geconcludeerd dat de helft van de Europeanen stierf lang voordat de pest de uitgedunde en uitgeputte bevolking verliet.
De tweede pandemie, vooral bekend als de Zwarte Dood, begon zijn aanval op Europa in 1346. Geïntroduceerd vanaf Oost-China volgens de Grote zijderoute naar de Krim verspreidde de infectie zich snel naar het noorden en eiste binnen vier jaar het leven van meer dan 25 miljoen mensen, wat op dat moment een derde van de gehele Europese bevolking bedroeg. De ziekte gaf vier eeuwen lang niet op - hij verborg zich of laaide op (vooral in grote steden), zwervend van land naar land. In 1665–1666 stierf een op de vijf Londenaren aan de builenpest; maar ondanks de betreurenswaardige situatie bleef de geneeskunde machteloos.
Gezichten van de pest
Momenteel zijn de belangrijkste vormen van pest builenpest, long En septisch. Af en toe worden ook andere varianten aangetroffen: huid-, darm-, keel- en meningeale soorten. De builenpest ontstaat meestal na de beet van een vlo die de pest bij zich draagt Y. pestis of na het hanteren van karkassen van besmette dieren en wordt gekenmerkt door ontsteking lymfeklieren met de vorming van hun pijnlijke conglomeraten - "buboes", "kegels" verschillende maten. Als de behandeling niet op tijd wordt behandeld, kan de infectie zich veralgemenen: er ontstaat sepsis (secundaire bloedvergiftiging) of longontsteking (secundaire longpest). In het laatste geval dient het sputum als een besmettelijke substantie voor andere mensen, die vervolgens een primaire longpest ontwikkelen. Juist vanwege het vermogen om van persoon op persoon te worden overgedragen (via druppeltjes in de lucht), veroorzaakt de longvorm van de ziekte de grootste zorg. Septische en longvormen komen soms razendsnel voor en de dood kan niet worden vermeden zonder noodbehandeling met antibiotica.
Het is mogelijk dat de overheersing van welke vorm van pest dan ook (overheersende schade aan een of ander orgaan) tijdens verschillende epidemieën niet alleen verband houdt met de mechanismen van bacteriële overdracht, maar ook met de eigenschappen van een bepaalde pathogene stam.
Slachtoffer van mutatie
Het is al geruime tijd bekend dat de voorouder van de pestbacil is Yersinia pseudotuberculose- enteropathogeen, veroorzaker van pseudotuberculose. Vermoedelijk Y. pestis ongeveer twintigduizend jaar geleden gescheiden van zijn voorouderlijke soort. De reden voor de evolutie was een scherpe klimaatverandering in het late Pleistoceen (de Quartaire periode van het Cenozoïcum): kou werd vervangen door hitte, wat een herstructurering van ecosystemen veroorzaakte; In de regel stimuleren dergelijke ‘sprongen’ in het weer de evolutie van soorten. Tot voor kort waren de genetische veranderingen die van cruciaal belang zijn voor de transformatie van een ziekteverwekker die een infectieuze darmziekte veroorzaakt in een gevaarlijk micro-organisme dat de longen kan infecteren en fulminante sepsis kunnen veroorzaken, echter niet bekend.
Evolutionaire tak Y. pestis werd bestudeerd door wetenschappers van de Northwestern University in de VS. In een onderzoek van Wyndham Lathem en Daniel Zimbler ontdekten ze dat de verwerving van één enkel gen vroege vormen transformeerde Y. pestis, genetisch en fenotypisch al enigszins verschillend van Y. pseudotuberculose, tot een succesvol longpathogeen. Om het mechanisme van de ‘verplaatsing’ van de pestbacil van de darmen naar de longen te identificeren, voerden de auteurs experimenten uit met oude bacteriestammen en analyseerden ze hun gedrag in het lichaam van muizen. Bij het vergelijken van stammen die longpest veroorzaken met relatief onschadelijke voorouders, werd slechts één, maar zeer significant verschil onthuld: verwerving van het oppervlaktegen werd van cruciaal belang eekhoorn Pla (cm. doos) als onderdeel van het pPCP1-plasmide. Om de hypothese te testen werd dit gen geïntroduceerd in het DNA van evolutionair eerdere stammen - en de resultaten bevestigden de betrokkenheid van het Pla-protease bij effectieve schade aan de luchtwegen.
Echter, deze overname Y. pestis het was niet genoeg om te leren hoe je de gevaarlijkste systemische infectie (septische vorm van de pest) kon veroorzaken. Het bleek dat een dergelijke verbetering nodig was slechts één (!) aminozuursubstitutie in het Pla-eiwit - I259T . Deze vervanging optimaliseerde de proteolytische activiteit van het eiwit en verhoogde het invasieve potentieel van bacteriën tijdens de ontwikkeling van de builenpest aanzienlijk. Wetenschappers geloven dus dat de bacterie in de eerste plaats de eigenschappen heeft verworven van een longpathogeen, een provocateur uitbraken longpest, en later, als gevolg van een extra mutatie, verschenen er nog gevaarlijkere stammen die de oorzaak waren pandemie pulmonale bloedvergiftiging en builenziekte.
Echter, tussen alle nadelen Y. pestis Wetenschappers vinden ook voordelen van haar contact met mensen. In 2014 in het tijdschrift PLoS EEN Er werd een artikel gepubliceerd door Sharon de Witte van de Universiteit van South Carolina, waarin werd gesteld dat mensen die de pestpandemie overleefden, eigenaar werden van meer goede gezondheid. Wetenschappers hebben de overblijfselen van mensen die vóór, tijdens en na de pest leefden, tekenend onderzocht Speciale aandacht over de doodsoorzaken en de toestand van hun botten. De resultaten toonden aan dat overlevenden van de epidemie, evenals hun nakomelingen, gemiddeld 75 jaar leefden en een benijdenswaardige immuniteit hadden.
Iets over Pl
Figuur 1. Mechanisme van preventie van apoptose door Pla-protease Y. pestis. Links- normale Fas-signalering wanneer Pla is geïnactiveerd, rechts- onderdrukking van apoptose door het “werkende” protease. FasL- transmembraaneiwit gelokaliseerd op het oppervlak van lymfocyten; Fas- FasL-receptor; Pla- een protease ingebouwd in het buitenmembraan van de bacteriecel. Tekening van.
Waarom wordt het Pla-protease geclassificeerd als een virulentiefactor, d.w.z. hoe precies Heeft ze de pestbacil geholpen, die al beschikt over een rijk arsenaal aan aanpassingen om goed te gedijen bij zoogdieren en overgedragen te worden door vlooien? Een van Pla's verantwoordelijkheden is plasminogeen activatie: het resulterende plasmine vernietigt fibrinestolsels, wat bijvoorbeeld belangrijk is voor de verspreiding van bacteriën uit builen door het lichaam.
Onlangs is de ontwikkeling van primaire longinfecties in verband gebracht met een mechanisme dat hiermee verband houdt inactivatie van een apoptotisch signaalmolecuul genaamd Fas-ligand(FasL). De rol van FasL in de cel wordt bepaald door zijn vermogen om het proces van apoptose op gang te brengen. Dit eiwit, dat het membraan van geactiveerde cytotoxische T-lymfocyten en epitheelcellen van de luchtwegen omspant, heeft een extracellulair domein dat zich bindt aan de FasR-receptor op het oppervlak van andere cellen (voornamelijk lymfocyten, maar ook hepatocyten, kanker en enkele andere), die door activering van caspase-proteasen, 8 en caspase-3/7 veroorzaken apoptose. Dit handhaaft de homeostase van immunocyten, voorkomt auto-immuunprocessen en vernietigt cellen die vreemde antigenen tot expressie brengen.
Pla-protease katalyseert de splitsing van het FasL “werkende” domein op verschillende plaatsen en inactiveert daardoor dit eiwit – zowel de membraan- als de oplosbare vormen. Zo voorkomt Pla apoptose en aanverwante zaken ontstekingsreacties, noodzakelijk voor een volledige immuunrespons, die bijdraagt aan de overleving van de ziekteverwekker in het gastheerlichaam (Fig. 1).
Experimenten uitgevoerd op muizen lieten het volgende zien: bacteriën met normaal Pla-protease droegen bij aan een afname van de hoeveelheid FasL, wat leidde tot snelle kolonisatie van de longen, terwijl Yersinia met geïnactiveerd Pla zich langzamer vermenigvuldigde. Het beschreven mechanisme voor het onderdrukken van de immuunrespons kan volgens wetenschappers vooral door andere pathogenen worden gebruikt infecties veroorzaken luchtwegen. En dit opent op zijn beurt nieuwe perspectieven in de strijd tegen dergelijke ziekten: je kunt bijvoorbeeld denken aan de ontwikkeling van Pla-remmers of de introductie van extra FasL-moleculen.
"Taxi naar huis"
Hoofdvervoerder Y. pestis van knaagdieren naar mensen is de vlo (Fig. 2), en voor het insect is dit een gedwongen "passagierslevering", waarvan de prijs het leven van de "vervoerder" is.

Figuur 2. Een vlo klampt zich vast aan de vacht van een rat. De foto werd genomen met behulp van een elektronenmicroscoop en er werd kleuring aangebracht. Figuur van science.nationalgeographic.com.
Vlooien zijn vraatzuchtige bloedzuigers. De voeding van een individu kan één minuut tot meerdere uren duren; sommige soorten slagen erin hun magen zo goed mogelijk te vullen, zozeer zelfs dat ze niet eens de tijd hebben om hun bloedige lunch te verteren. Misschien was het dit feit dat een wrede grap met de insecten uithaalde, maar het had niet op een geschikter moment kunnen gebeuren. Y. pestis.
De pestbacil komt tijdens het voeden het lichaam van de vlo binnen en hoopt zich op in het gewas, waar hij zich intensief begint te vermenigvuldigen. In dit geval vormen de bacteriën een soort biofilm: een meerlaagse ophoping van cellen ondergedompeld in een exopolysacharidematrix. Dit fenomeen werd zelfs het ‘pestblok’ genoemd. Dus wanneer de vlo zich vervolgens voedt, komt er geen bloed in de maag - het insect heeft honger en gaat vaker 'op jacht'. Geïnfecteerde vlooien leven niet lang (dit is begrijpelijk - je kunt niet ver rennen zonder voedsel), maar gedurende deze tijd slagen ze erin ongeveer 15 dieren, inclusief mensen, te infecteren.
Dit gebeurt als volgt. Omdat het bloed niet voorbij de biofilm komt, hoopt het zich op in de slokdarm en de krop. Wanneer een vlo een slachtoffer bijt, kan er simpelweg nergens een nieuwe portie voedsel naartoe, en een deel van de vorige maaltijd van het insect samen met een portie bacteriën Y. pestis komt in de wond terecht. De baby heeft slechts een uur nodig om het lichaam van de ongelukkige te 'omzeilen' en, samen met de bloedbaan, de milt, lever en longen binnen te dringen. Incubatietijd(de tijd vanaf de penetratie van de ziekteverwekker in het lichaam tot de eerste klinische manifestaties) duurt van enkele uren tot 12 dagen. Het transmissiediagram van de ziekteverwekker* wordt weergegeven in Figuur 3.
* - Helaas kan een mens met een vlo concurreren als het gaat om de verfijning van de mechanismen voor de verspreiding van infecties. De laatste grote pestepidemie vond plaats in Verre Oosten in 1910-1911, maar er komen nog steeds lokale uitbraken voor - de pest is niet volledig verslagen Een ander ding is dat antibiotica nu bijna overal verkrijgbaar zijn. Maar hoe werden uitbraken geëlimineerd vóór het ‘antibioticatijdperk’? Een opmerkelijk verhaal over de strijd tegen de pest in Sovjet Hadrut (1930) werd verteld door de briljante viroloog en arts Lev Zilber in zijn memoires “ Operatie "ORE"". Dit is een echt medisch (en zelfs een beetje spionage - vanwege de speciale kijk van de “partij en de regering” op dergelijke gebeurtenissen) detectiveverhaal, zowel spannend als tragisch, dat je doet nadenken over het concept van “dokter”, de eigenaardigheden van het tijdperk en onzelfzuchtig werk in tegenstelling tot alles (de wreedheid van de bevolking, de wreedheid van de leiding van het land, enz.). De oorzaak van de uitbraak kon toen nog worden vastgesteld. Maar... wat een vlooien zijn er! Wij raden het ten zeerste aan om het te lezen. - Ed.
"Ik geloof het, ik geloof het niet"
Rondom Y. pestis Er doen veel geruchten en mythen de ronde. De bacterie werd bijvoorbeeld beschouwd als de boosdoener van de “Pest van Athene” - een epidemie die in het tweede jaar van de Peloponnesische Oorlog door het oude Athene trok. De toestroom van vluchtelingen naar de Griekse stad veroorzaakte overbevolking en overbevolking, wat ongetwijfeld heeft bijgedragen aan onhygiënische omstandigheden: er was geen tijd om toezicht te houden op de hygiëne, aangezien de belangrijkste strijdkrachten erop gericht waren militaire superioriteit over de vijanden te bereiken. Onder deze omstandigheden ontstond er een epidemie van ‘pest’, die door de Grieken werd gezien als een goddelijke straf voor de familievloek van de Alcmaeoniden. Modern onderzoek bewijst echter de niet-betrokkenheid Y. pestis tot een epidemie in het oude Griekenland. Met behulp van moleculair genetische analyse werd vastgesteld dat de tanden* gevonden in de begrafenissen van slachtoffers van de Atheense epidemie geen DNA van de pestbacil bevatten, maar DNA van bacteriën. Salmonella typhi- ziekteverwekker buiktyfus.
* - Meer over hoe DNA uit tanden wordt gehaald, kun je lezen in het artikel “ » .
Verdere controverse ontstaat rond "assistenten" in de distributie Y. pestis. De ziekte wordt overgedragen door vlooien en vlooien worden overgedragen door knaagdieren. Men geloofde dat Europese ratten (Fig. 4), ooit besmet met de pest, eeuwenlang als infectiereservoir hebben gediend, maar dit feit wordt nu betwist door Noorse wetenschappers. Nils Christian Stenseth van de Universiteit van Oslo legt uit dat uitbraken van de pest gepaard moeten gaan met weersschommelingen: vooral warme en vochtige lente-zomerperioden worden gekenmerkt door een snelle ontwikkeling van planten en een overvloed aan voedsel, het aantal knaagdieren neemt in dergelijke jaren aanzienlijk toe , wat betekent dat de pest zich sneller verspreidt. Een studie van oude gegevens over de klimaatverandering in Europa en Azië tijdens pandemieën leidde tot de conclusie dat in Europa het uitbreken van epidemieën inderdaad overeenkwam met gunstige natuurlijke omstandigheden, maar alleen... in Azië en met een stabiele vertraging van ongeveer 15 jaar. Hieruit konden we concluderen dat de pestbacil eeuwenlang niet verborgen was in Europese ratten, maar keer op keer door handelaren uit Azië werd geïmporteerd. Is het waar, deze hypothese vereist nog steeds strikte wetenschappelijke bevestiging - Stenset is van plan uit te voeren genetische analyse de overblijfselen van slachtoffers van Europese pestuitbraken en vergelijk de genomen van ziekteverwekkers;
Pest stok(Yersinia pestis) - een type gramnegatieve sporogene bacteriën, facultatieve anaëroben. De veroorzaker van de builenpest, longontsteking (longpest) en bloedvergiftiging.
Plaag van de mens
Bij mensen wordt de pest gekenmerkt door een plotselinge temperatuurstijging en malaise, die gepaard kan gaan met buikpijn, misselijkheid en braken. Er zijn drie hoofdvormen van pest, afhankelijk van de infectiemethode: Het sterftecijfer voor de pest, indien onbehandeld, varieert van 63% tot 93%. Tijdens de behandeling moderne antibiotica- ongeveer 16%. Tijdige behandeling met antimicrobiële geneesmiddelen zoals aminoglycosiden, fluorochinolonen of doxycycline vergroot de kans op een gunstig resultaat aanzienlijk.
Het sterftecijfer voor de pest, indien onbehandeld, varieert van 63% tot 93%. Tijdens de behandeling moderne antibiotica- ongeveer 16%. Tijdige behandeling met antimicrobiële geneesmiddelen zoals aminoglycosiden, fluorochinolonen of doxycycline vergroot de kans op een gunstig resultaat aanzienlijk. In de XIV-XVII eeuw stierven in Europa volgens verschillende schattingen 50 tot 75 miljoen mensen aan de builenpest. De laatste uitbraak van de pest werd in de zomer van 2015 in Madagaskar geregistreerd.
Menselijke plaag in de VS
Volgens een bericht van de Centers for Disease Control and Prevention (CDC), VS, gedateerd 25 augustus 2015, werden tussen 2001 en 2012 in de Verenigde Staten jaarlijks tussen de 1 en 17 gevallen van de pest bij mensen gemeld (een gemiddelde van drie gevallen per jaar ). Gedurende de periode van 1 april 2015 (tot 25 augustus 2015) werden 11 gevallen van menselijke pest gerapporteerd in 6 staten (veroorzaker Yersinia pestis). Er zijn twee gevallen in verband gebracht met bezoeken aan het Yosemite National Park in Californië. 3 patiënten (leeftijd 16, 52 en 79 jaar) overleden. De reden voor de scherpe toename van de pestincidentie in de Verenigde Staten in 2015, zoals vermeld in het genoemde persbericht, is niet duidelijk.Yersinia pestis in ICD-10
Yersinia pestis wordt vermeld in de Internationale Classificatie van Ziekten ICD-10 in “Klasse I. Sommige infectie- en parasitaire ziekten”, in het blok “A20-A28 Sommige bacteriële zoönosen”, waar een kop van drie tekens staat “A20 Pest” met een uitleg , dat het een infectie omvat die wordt veroorzaakt door Yersinia pestis. Deze categorie omvat categorieën van vier tekens:
dat het een infectie omvat die wordt veroorzaakt door Yersinia pestis. Deze categorie omvat categorieën van vier tekens: - A20.0 Builenpest
- A20.1 Cellulocutane plaag
- A20.2 Longpest
- A20.3 Pest-meningitis
- A20.7 Septicemische plaag
- A20.8 Overige vormen van pest (met interpretatie: mislukte pest. Asymptomatische pest. Kleine pest)
- A20.9 Pest, niet gespecificeerd
Heeft een kleine mutatie in Yersinia pestis de menselijke geschiedenis veranderd?
In een artikel uit 2015, gepubliceerd in het tijdschrift Nature Communications, zegt Dr. D.Zimbler en Dr. W. Lathem van de Northwestern University (VS) beschreef de enige die ze ontdekten genetische eigenschap Yersinia pestis, die de loop van de evolutie van micro-organismen en de geschiedenis van de mensheid fundamenteel veranderde. In het verleden Yersinia pestis konden geen pneumonische vormen van pest veroorzaken. De verwerving van een enkel gen voor het oppervlakte-eiwit Pla leidde tot de transformatie Yersinia pestis van een ziekteverwekker die darminfectieziekten veroorzaakt tot een micro-organisme dat geassocieerd is met de ontwikkeling van ernstige en dodelijke infecties ademhalingsorganen.Rol Yersinia pestis in De Zwarte Dood wordt besproken. Sommigen beweren dat de Zwarte Dood zich te snel verspreidde om veroorzaakt te kunnen worden Yersinia pestis. Het DNA van deze bacterie werd gevonden in de tanden van degenen die stierven aan de Zwarte Dood, terwijl het testen van middeleeuwse overblijfselen van mensen die door andere oorzaken stierven niet aan het licht kwam positieve reactie op Yersinia pestis. Dit bewijst dat Yersinia pestis is op zijn minst een factor die bijdraagt aan sommige (misschien niet alle) Europese pestepidemieën. Het is mogelijk dat selectie door de pest de pathogeniteit van de bacterie zou kunnen beïnvloeden, waardoor individuen zouden worden geëlimineerd die er het meest vatbaar voor waren.
Verkrijgbaar in Rusland levend vaccin gebaseerd op een niet-virulente peststam.
Genoom
Van verschillende ondersoorten van de bacterie zijn volledige genetische sequenties beschikbaar: stam KIM (van biovar Medievalis), stam CO92 (van biovar Orientalis verkregen uit een klinische isolatiefaciliteit in de VS), stam Antiqua, Nepal516, Pestoides F. De chromosomen van stam KIM bestaat uit 4.600.755 basenparen, in stam CO92 - 4.653.728 basenparen. Zoals familieleden Y. pseudotuberculose En Y. enterocolitica, bacteriën Y. pestis bevat plasmiden pCD1. Daarnaast bevat het ook plasmiden pPCP1 En pMT1, die niet voorkomen bij andere soorten van het geslacht Yersinia. De vermelde plasmiden en het genoemde pathogeniteitseiland HPI, coderen voor eiwitten die de oorzaak zijn van de pathogeniteit van de bacterie. Deze virulentiefactoren zijn onder andere nodig voor bacteriële adhesie en injectie van eiwitten in de gastheercel, bacteriële invasie van de gastheercel en opname en binding van ijzer verkregen uit rode bloedcellen.
Behandeling
Sinds 1947 wordt de traditionele eerste fase behandeling voor Y. pestis waren streptomycine, chlooramfenicol of tetracycline. Er zijn ook aanwijzingen dat het gebruik van doxycycline of gentamicine voordelen biedt.
Opgemerkt moet worden dat er stammen zijn geïsoleerd die resistent zijn tegen een of twee van de hierboven genoemde middelen en dat de behandeling, indien mogelijk, gebaseerd moet zijn op hun gevoeligheid voor antibiotica. Voor sommige patiënten is behandeling met antibiotica alleen niet voldoende en kan ondersteuning van de bloedsomloop, de ademhaling of de nieren nodig zijn.
Schrijf een recensie over het artikel "Peststok"
Opmerkingen
- Collins FM. Pasteurella, Yersinia en Francisella. In: Barron's medische microbiologie (Barron S et al , red.). - 4e druk.. - Universiteit van Texas Medical Branch, 1996. - ISBN.
- - een artikel gepubliceerd in het tijdschrift "Knowledge-Power" nr. 2 voor 2002 bevat gedachten waarin kritiek wordt geuit op het verband tussen bacteriën en de pest.
- Drancourt M; Aboudharam G; Signolidagger M; Dutourdolk O; Raoult D. (1998). "". PNAS 95 (21): 12637–12640.
- Drancourt M; Raoult D. (2002). "". Microben infecteren. 4 : 105–9.
- . Lenta.ru. Opgehaald op 23-10=2015.
- Daniel L. Zimbler, Jay A. Schroeder, Justin L. Eddy & Wyndham W. Lathem.. natuur.com. Opgehaald op 13-02=2016.
- . Lenta.ru. Opgehaald op 23-10=2015.
- Simon Rasmussen.. mobiel.com. Opgehaald op 13-02=2016.
- Salyers AA, Whitt DD. Bacteriële pathogenese: een moleculaire benadering. - 2e ed.. - ASM Press, 2002. - ISBN pp207-12.
- Welkos S et al.. (2002). "". Vaccin 20 : 2206–2214.
- title=Vaccinepest levend, droog | url=http://www.epidemiolog.ru/catalog_vac/index.php?SECTION_ID=&ELEMENT_ID=476
- Supotnitsky MV, Supotnitskaya NS, 2006,
- Supotnitsky MV, Supotnitskaya NS, 2006,
- Deng W et al.. (2002). "". Tijdschrift voor Bacteriologie 184 (16): 4601–4611.
- Parkhill J et al.. (2001). "". Natuur 413 : 523–527.
- Wagle PM. (1948). "Recente vooruitgang in de behandeling van de builenpest." Indiase J Med Sci 2 : 489–94.
- Meijer KF. (1950). "Moderne pesttherapie." JAMA 144 : 982–5.
- Kilonzo BS, Makundi RH, Mbise TJ. (1992). "Een decennium van geplaagde epidemiologie en controle in het westelijke Usambara-gebergte, in het noordoosten van Tanzania." Acta Tropica 50 : 323–9.
- Mwengee W, Butler T, Mgema S, et al.(2006). "Behandeling van de pest met gentamicine of doxycycline in een gerandomiseerde klinische proef in Tanzania." Clin Infect Dis 42 : 614–21.
De inhoud van het artikel
De naam wordt gegeven ter ere van A. Yersin. Het geslacht Yersinia omvat verschillende soorten, waarvan Y. pestis, Y. enterocolitica en Y. pseudotuberculosis pathogeen zijn voor de mens. Het zijn gramnegatieve, niet-sporenvormende staafjes. Ze onderscheiden zich door biochemische, antigene en andere kenmerken.
