Wymiary i waga prawidłowej tarczycy. Masa tarczycy i wpływ na masę ciała
Grasica (grasica lub grasica) to narząd ludzkiej odporności i hematopoezy, odpowiedzialny za syntezę niektórych rodzajów białych krwinek. Gruczoł znajduje się bezpośrednio za mostkiem, w śródpiersiu górnym. Rzadko występuje nietypowe ułożenie płatków grasicy na grubości Tarczyca, w tkance tłuszczowej tylnego śródpiersia lub pomiędzy mięśniami szyi. Taki układ nazywa się anormalnym i występuje u jednej czwartej światowej populacji. Czynnikiem predysponującym do nieprawidłowej lokalizacji grasicy jest wady wrodzone kiery.
Narząd ma różowo-szary kolor i miękką teksturę o płatkowej strukturze. Zdrowa grasica składa się z dwóch dużych płatów i ma kształt widelca z dwoma zębami, od czego wzięła się druga nazwa tego narządu. Uszkodzony gruczoł może zmienić swój kształt. Z góry płaty pokryte są torebką tkanki łącznej z mostkami sięgającymi do grubości gruczołu. Mostki dzielą płaty na mniejsze płaty. Masa gruczołu u noworodka i niemowlęcia wynosi około 15-17 g, wielkość nie przekracza 4-5 cm, a grubość 0,5 cm Grasica osiąga maksymalny rozmiar na początku okresu dojrzewania - 8-16 cm długości, a masa wzrosła dwukrotnie. Następnie u dorosłych gruczoł stopniowo ulega odwrotnemu rozwojowi - inwolucji - i praktycznie łączy się z otaczającą go tkanką tłuszczową. Inwolucja może być fizjologiczna (związana z wiekiem) i przypadkowa - pod wpływem stresującego działania na organizm.
Grasica jest zaopatrywana przez gałęzie tętnicy piersiowej wewnętrznej, aorty i tętnic tarczowych. Odpływ krwi odbywa się przez wewnętrzne żyły piersiowe i ramienno-głowowe. Jest unerwiony przez gałęzie nerwu błędnego i pień współczulny.
Histologia grasicy
Grasica rozwija się z ektodermy i zawiera komórki pochodzenia nabłonkowego i krwiotwórczego. Konwencjonalnie cała substancja grasicy dzieli się na korową i mózgową. Kora zawiera:
- komórki tworzące barierę hemato-grasiczą - komórki podporowe;
- komórki gwiaździste wydzielające hormony;
- komórki „niani”, pomiędzy procesami, w których rozwijają się i dojrzewają limfocyty T;
- Limfocyty T - białe krwinki;
- makrofagi grasicy.
Rdzeń zawiera dużą liczbę dojrzewających limfocytów T. Kiedy komórki te przechodzą przez wszystkie etapy rozwoju, są wysyłane do krwiobiegu przez żyły i żyły, gdzie są gotowe do pełnienia funkcji odpornościowych.
W ten sposób limfocyt T pojawia się i zaczyna dojrzewać w substancji korowej, a następnie w miarę dojrzewania przechodzi do rdzenia. Proces ten trwa około 20-22 dni.
W miarę przemieszczania się z kory do rdzenia i z rdzenia do krążenia ogólnego, limfocyty T podlegają selekcji – selekcji pozytywnej i negatywnej. W jego trakcie komórki „uczą się” rozpoznawać obcego i odróżniać swojego od obcego. Według naukowców jedynie 3-5% limfocytów T przechodzi oba etapy selekcji i dostaje się do krążenia ogólnoustrojowego. Selekcja pozwala określić, które z komórek w pełni spełniają swoją funkcję, a które nie muszą być uwalniane do krwioobiegu.
Jakie procesy reguluje grasica?
Główną rolą grasicy jest różnicowanie i dojrzewanie komórek odpornościowych limfocytów T – limfocytów T. Prawidłowy rozwój i selekcja tych komórek prowadzi do powstania wielu receptorów dla obcych substancji, a w efekcie do odpowiedzi immunologicznej w przypadku kontaktu z nimi.
Drugą funkcją grasicy jest synteza hormonów, takich jak:
- tymozyna;
- tymulina;
- tymopoetyna;
- insulinopodobny czynnik wzrostu-1;
- grasicowy czynnik humoralny.
Hormony grasicy wpływają na funkcję limfocytów T i stopień ich aktywności. Szereg badań wykazało aktywujący wpływ hormonów grasicy na ośrodkowy układ nerwowy.
tymozyna
Hormon ten jest białkiem polipeptydowym syntetyzowanym w komórkach nabłonkowych zrębu narządu i pełni takie funkcje jak:
- regulacja rozwoju układ mięśniowo-szkieletowy kontrolując metabolizm wapnia;
- regulacja metabolizmu węglowodanów;
- zwiększona synteza hormonów przysadkowych - gonadotropin;
- wzrost syntezy limfocytów T przed okresem dojrzewania;
- regulacja obrony przeciwnowotworowej.
Przy niewystarczającej aktywności lub wydzielaniu w organizmie człowieka rozwija się niewydolność limfocytów T - aż do absolutnego braku komórek. Klinicznie objawia się to gwałtownym spadkiem ochrony przed infekcjami, dominacją ciężkich i nietypowych postaci chorób zakaźnych.
tymopoetyna
Tymopoetyna jest hormonem peptydowym składającym się z 49 aminokwasów. Bierze udział w różnicowaniu i dojrzewaniu limfocytów T w korze i rdzeniu oraz określa, w którym z kilku typów limfocytów T dojrzewa dana komórka.
Inną funkcją hormonu jest blokowanie transmisji nerwowo-mięśniowej. Ma również właściwość immunomodulacji - jest to zdolność hormonu, jeśli to konieczne, do tłumienia lub wzmacniania syntezy i aktywności komórek T.
Timulina
Hormon białkowy, tymulina, wpływa na końcowe etapy różnicowania komórek T. Stymuluje dojrzewanie komórek i rozpoznawanie obcych czynników.
Spośród ogólnego wpływu na organizm zwiększa się ochrona przeciwwirusowa i antybakteryjna poprzez zwiększenie produkcji interferonów i nasilenie fagocytozy. Tymulina przyspiesza także regenerację tkanek. Oznaczenie tymuliny ma decydujące znaczenie w ocenie skuteczności leczenia chorób grasicy.
Inne hormony
Na swój sposób struktura chemiczna Insulinopodobny czynnik wzrostu-1 jest podobny do insuliny. Reguluje mechanizmy różnicowania, rozwoju i wzrostu komórek, uczestniczy w metabolizmie glukozy. W komórkach mięśniowych hormon ma działanie stymulujące wzrost, jest w stanie zmienić metabolizm i sprzyjać zwiększonemu spalaniu tłuszczu.
Czynnik humoralny grasicy odpowiada w organizmie za stymulację reprodukcji limfocytów.
Choroby grasicy
Choroby grasicy praktycznie nie występują u dorosłych, najczęściej patologię obserwuje się u dzieci w wieku poniżej jednego roku. Do najpowszechniejszych i najlepiej zbadanych chorób grasicy należą:
- zespół MEDAC;
- zespół DiGeorge’a;
- miastenia;
- różne nowotwory.
Zapalenie zrębu grasicy jest rzadkie.
Do nowotworów grasicy zalicza się:
- grasiczaki i rozrosty - łagodne nowotwory, w których gruczoł jest powiększony;
- hipoplazja lub niedorozwój narządu;
- chłoniak z komórek T;
- nowotwory pre-T-limfoblastyczne z przemianą w białaczkę lub nowotwór;
- nowotwory neuroendokrynne.
Choroby grasicy mają różnorodne objawy kliniczne, ale niektóre objawy są wspólne dla wszystkich:
- niewydolność oddechowa;
- ciężkość powiek;
- chroniczne zmęczenie;
- osłabienie mięśni i rzadko ból mięśni;
- obniżona odporność na infekcje.
Większość chorób grasicy jest niebezpieczna dla życia dziecka, dlatego w przypadku podejrzenia patologii grasicy konieczna jest pilna konsultacja z immunologiem i hematologiem.
Plan badań lekarskich obejmuje:
- ogólne i analizy biochemiczne krew;
- oznaczanie aktywności hormonów grasicy;
- immunogram;
- USG gruczołu.
Co to jest guzek koloidalny tarczycy?
Guzek koloidalny tarczycy, co to jest? Jest to patologia charakteryzująca się pojawieniem się łagodnych nowotworów. Ich obecność nie jest niebezpieczna dla życia człowieka, ale odgrywa ważną rolę w diagnostyce chorób układu hormonalnego. Węzły koloidalne w tarczycy występują u większości pacjentów endokrynologów, ale najczęściej są one łagodne. Koloid jest lepką masą wypełniającą pęcherzyk gruczołu, dlatego nie jest uważany za nietypowy dla to ciało. Taka substancja powstaje w tkankach odpowiedzialnych za produkcję hormonów tarczycy. Analiza mikroskopowa wykazuje, że węzeł składa się z komórek gruczołowych, krwi i koloidu. Nie zawiera obcych wtrąceń, co oznacza, że jest bezpieczny dla zdrowia.
Przyczyny rozwoju choroby
Rola tarczycy w organizmie człowieka jest nie do przecenienia. Narząd, który jest stosunkowo mały, musi wytwarzać wiele hormonów rozprowadzanych po całym organizmie. Chroniczne i choroba zakaźna, stres, niesprzyjające warunki środowiskowe powodują, że gruczoł pracuje w przyspieszonym tempie, co prowadzi do zaburzeń organicznych i funkcjonalnych. Niektóre części ciała zaczynają nierównomiernie wytwarzać hormony, czemu towarzyszy rozszerzenie naczyń i wzrost gęstości tkanki. W ten sposób powstają węzły koloidalne tarczycy.
Głównymi przyczynami powstawania węzłów koloidowych w tarczycy są: niekorzystne warunki środowiskowe, stres, duża aktywność fizyczna, choroby przewlekłe, niedobór jodu w organizmie, niedożywienie, okres dojrzewania, ciąża. Niedobór jodu jest najczęstszą przyczyną zmian guzkowych. Niedobory tego pierwiastka mają wszyscy mieszkańcy naszego kraju, z wyjątkiem ludności zamieszkującej Krym i Daleki Wschód. Rozważany jest jod istotna substancja, bez którego tarczyca nie jest w stanie wytwarzać hormonów.
Obraz kliniczny
We wczesnych stadiach rozwoju węzła nie pojawiają się żadne objawy. Częściej powodem udania się do lekarza jest znaczny wzrost wielkości gruczołu. W tym przypadku pojawiają się objawy mechanicznego oddziaływania węzła na otaczające tkanki: ucisk w okolicy narządu, trudności w połykaniu i oddychaniu, ból gardła, kaszel. NA późne etapy choroba zmienia barwę i głośność głosu. Ciągłe ściskanie dużych naczyń i zakończeń nerwowych może wpływać na centralny układ nerwowy: pojawiają się bóle głowy, zawroty głowy, szum w uszach. Ból szyi pojawia się wraz z szybkim wzrostem wielkości węzła, dodaniem krwotoków lub procesy zapalne.
W zależności od częstości występowania procesu patologicznego tarczyca może wzrosnąć zarówno po jednej, jak i po obu stronach. Jeśli wielkość węzła przekracza 1 cm, osoba może go wykryć samodzielnie. W zależności od stopnia dysfunkcji tarczycy obraz kliniczny choroby może być różny. Objawy niedoczynności tarczycy pojawiają się, gdy masa koloidalna zaczyna zastępować zdrowe komórki gruczołu. Pojawia się ogólne osłabienie, maleje zdolność intelektualna utrata apetytu. Ciało pacjenta puchnie, procesy metaboliczne w organizmie zwalniają, waga zaczyna rosnąć, skóra staje się sucha.
Kiedy tarczyca zaczyna wytwarzać zwiększoną ilość hormonów, dana osoba doświadcza objawów nadczynności tarczycy. Stan ten objawia się drażliwością, zmęczeniem, agresją. Apetyt wzrasta, ale osoba traci na wadze, procesy trawienne są zaburzone, co objawia się biegunką. Temperatura ciała może wzrosnąć i rozwinąć się tachykardia. Jeśli proces produkcji hormonów nie zostanie zakłócony, jedyną oznaką choroby będzie zagęszczenie tarczycy i jej powiększenie. Rosnące węzły uciskają duże naczynia i zakończenia nerwowe, co prowadzi do uczucia guza w gardle, problemów z oddychaniem i połykaniem.
Diagnostyka i leczenie choroby
Naturę węzłów w tarczycy można określić dopiero po pełne badanie. Rozpoczyna się od palpacji okolicy szyjnej, w której wykrywane są zmiany patologiczne. Dodatkowe metody diagnostyczne obejmują: biopsję, USG tarczycy, CT lub MRI, badanie krwi na obecność hormonów, skanowanie radioizotopowe. Na podstawie wyników procedury diagnostyczne endokrynolog stwierdza obecność zmian organicznych i czynnościowych w tarczycy. Biopsję zaleca się w obecności dużych węzłów koloidowych. Pomimo tego, że w większości przypadków zmiany węzłowe mają charakter łagodny, konieczne jest zbadanie struktury największego z nich.

W przypadku bezobjawowego przebiegu procesu patologicznego leczenie może nie rozpocząć się natychmiast. Zaleca się obserwację nowotworu przez kilka lat. Lekarz może przepisać preparaty jodu w celu przywrócenia funkcji tarczycy. Pacjent może chcieć pozbyć się guzka koloidalnego chirurgicznie Jednak lekarze nie zalecają takich operacji. Po resekcji tkanka tarczycy zaczyna rosnąć szybciej.
Interwencję chirurgiczną należy przeprowadzić, jeśli istnieją bezwzględne wskazania: ucisk przez węzeł dużych naczyń i zakończeń nerwowych, produkcja zwiększonej ilości hormonów. Radykalne operacje są również stosowane w złośliwym charakterze przebiegu procesu patologicznego. W zależności od wielkości guza i obecności przerzutów tarczycę można usunąć częściowo lub całkowicie.
W pozostałych przypadkach leczenie węzłów koloidowych rozpoczyna się od wyeliminowania przyczyny ich powstawania. Na przykład, jeśli wole toksyczne przyczyniło się do gromadzenia masy koloidalnej, konieczne jest uregulowanie produkcji hormonów tarczycy i przywrócenie funkcji wszystkich narządów i układów. Jeżeli przyczyna zmian guzkowych nie została wyjaśniona, prowadzi się terapię objawową, mającą na celu wyeliminowanie nieprzyjemnych wrażeń związanych z mechanicznym działaniem węzła koloidalnego na otaczające tkanki.
Istnieje kilka sposobów leczenie zachowawcze: terapia lekowa mająca na celu wyeliminowanie dysfunkcji tarczycy; małoinwazyjne interwencje chirurgiczne - leczenie laserowe lub stwardnienie węzłów chłonnych. Przed przepisaniem konkretnego leku należy wykonać badanie krwi na obecność hormonów, aby ocenić funkcjonalność narządu. Pacjenta należy zapytać o obecność reakcji alergicznych na leki. W większości przypadków przepisywane są pochodne tyroksyny i tarczycy.
Właściwie dobrany schemat leczenia pozwala uniknąć rozwoju niebezpiecznych powikłań. Węzły koloidalne są zjawiskiem dość powszechnym, nie ma konkretnych środków zapobiegawczych. Osoba powinna uważnie monitorować swój stan zdrowia, regularnie odwiedzać endokrynologa, dobrze się odżywiać i przyjmować preparaty jodu. Należy unikać narażenia na promieniowanie i odwiedzania miejsc o niekorzystnym działaniu sytuację środowiskową. Pomoże to w utrzymaniu zdrowia tarczycy, normalizacji struktury jej tkanek i poprawie ogólnego stanu organizmu.
Funkcje hormonalne tarczycy i ich zaburzenia
Lokalizacja
Łącząc odchylenia od normy w ich stanie z patologią tarczycy, pacjenci zastanawiają się, gdzie znajduje się tarczyca, ponieważ diagnoza zaczyna się od tego - od palpacji.

Gruczoł znajduje się pod krtani, na poziomie piątego lub szóstego kręgu szyjnego. Pokrywa górną część tchawicy płatami, a przesmyk gruczołu wpada bezpośrednio do środka tchawicy.
Kształt gruczołu przypomina motyla ze skrzydłami zwężającymi się ku górze. Lokalizacja nie zależy od płci, w jednej trzeciej przypadków może występować niewielka dodatkowa część gruczołu w postaci piramidy, która nie wpływa na jego funkcjonowanie, jeśli występuje od urodzenia.
Wagowo tarczyca osiąga 25 gramów i nie więcej niż 4 cm długości, średnia szerokość wynosi 1,5 cm, ta sama grubość. Objętość mierzona jest w mililitrach i wynosi do 25 ml dla mężczyzn i do 18 ml dla kobiet.
Funkcje
Tarczyca to narząd wydzielania wewnętrznego odpowiedzialny za produkcję hormonów. Funkcje tarczycy obejmują regulację hormonalną poprzez produkcję określonego rodzaju hormonów. Hormony tarczycy zawierają w swoim składzie jod, ponieważ inną funkcją gruczołu jest magazynowanie i biosynteza jodu do bardziej aktywnej funkcji organicznej.

Hormony gruczołów
Pacjenci kierowani na diagnostykę laboratoryjną chorób tarczycy błędnie sądzą, że badają hormony tarczycy: TSH, AT-TPO, T3, T4, kalcytoninę. Ważne jest, aby rozróżnić, które hormony są produkowane przez tarczycę, a które są innymi narządami wydzielania wewnętrznego, bez których tarczyca po prostu nie będzie działać.
- TSH to hormon stymulujący tarczycę wytwarzany przez przysadkę mózgową, a nie tarczycę. Ale reguluje pracę tarczycy, aktywuje wychwytywanie jodu z osocza krwi przez tarczycę.
- Ab-TPO jest przeciwciałem przeciwko tyroperoksydazie, niehormonalnej substancji wytwarzanej przez układ odpornościowy w wyniku procesów patologicznych i chorób autoimmunologicznych.
Bezpośrednio hormony tarczycy i ich funkcje:
- Tyroksyna - T4 lub tetrajodotyronina. Reprezentuje hormony tarczycy, odpowiada za metabolizm lipidów, obniżając stężenie trójglicerydów i cholesterolu we krwi, wspomaga metabolizm tkanki kostnej.
- Trójjodotyronina – T3, główny hormon tarczycy, ponieważ tyroksyna również ma tendencję do przekształcania się w trójjodotyroninę poprzez przyłączenie innej cząsteczki jodu. Odpowiada za syntezę witaminy A, obniżanie stężenia cholesterolu, aktywację metabolizmu, przyspieszanie metabolizmu peptydów, normalizację pracy serca.
- Tyrokalcytonina nie jest specyficznym hormonem, ponieważ może być również wytwarzana przez grasicę i gruczoł przytarczyczny. Odpowiada za gromadzenie i dystrybucję wapnia w organizmie tkanka kostna zasadniczo go wzmacniając.

Na tej podstawie można stwierdzić, że jedyną rzeczą, za którą odpowiada tarczyca, jest synteza i wydzielanie hormonów tarczycy. Ale wytwarzane przez nią hormony pełnią szereg funkcji.
proces wydzielania
Praca tarczycy nie zaczyna się nawet w samym gruczole. Proces produkcji i wydzielania rozpoczyna się przede wszystkim od „poleceń” mózgu dotyczących braku hormonów tarczycy, a tarczyca je realizuje. Algorytm wydzielania można opisać w następujących krokach:
- Po pierwsze, przysadka mózgowa i podwzgórze otrzymują sygnał z receptorów, że poziom tyroksyny i trójjodotyroniny we krwi jest niski.
- Przysadka mózgowa wytwarza TSH, który aktywuje wychwyt jodu przez komórki tarczycy.
- Żelazo wychwytując nieorganiczną formę jodu pozyskiwaną z pożywienia, rozpoczyna swoją biosyntezę do bardziej aktywnej, organicznej formy.
- Synteza zachodzi w pęcherzykach tworzących trzon tarczycy, które są wypełnione płynem koloidalnym zawierającym tyreoglobulinę i peroksydazę do syntezy.
- Powstała organiczna forma jodu przyłącza się do tyreoglobuliny i uwalnia do krwi. W zależności od liczby przyłączonych cząsteczek jodu powstaje tyroksyna – cztery cząsteczki jodu lub trójjodotyronina – trzy cząsteczki.
- We krwi T4 lub T3 są uwalniane niezależnie od globuliny i są ponownie wychwytywane przez komórki gruczołów do wykorzystania w dalszej syntezie.
- Receptory przysadki mózgowej otrzymują sygnał o wystarczającej ilości hormonów, produkcja TSH staje się mniej aktywna.
W związku z tym, po wykryciu objawów choroby tarczycy, lekarz przepisuje badanie nie tylko stężenia hormonów tarczycy, ale także hormonów, które je regulują, a także przeciwciał przeciwko ważnemu składnikowi koloidu - peroksydazie.
aktywność gruczołów
NA ten moment Medycyna dzieli wszystkie patologie tarczycy na trzy stany:
- Nadczynność tarczycy to zaburzenie czynności tarczycy, w którym wzrasta aktywność wydzielnicza, a do krwi przedostaje się nadmiar hormonów tarczycy, wzmagają się procesy metaboliczne w organizmie. Do choroby zalicza się także tyreotoksykozę.
- Niedoczynność tarczycy to dysfunkcja tarczycy, w wyniku której wytwarzana jest niewystarczająca ilość hormonów, w wyniku czego procesy metaboliczne ulegają spowolnieniu z powodu braku energii.
- Eutyreoza - choroby gruczołu jako narządu, które nie mają żadnych objawów hormonalnych, ale towarzyszy im patologia samego narządu. Wśród chorób obejmuje to rozrost, wole, formacje guzkowe.

Choroby tarczycy u kobiet i mężczyzn diagnozuje się na podstawie wskaźnika TSH, którego spadek lub wzrost wskazuje na reaktywność lub niedoczynność gruczołu.
Choroby
U kobiet objawy chorób tarczycy pojawiają się częściej, gdyż wahania hormonalne odbijają się na cyklu menstruacyjnym, co powoduje, że pacjentka szuka pomocy lekarskiej. Mężczyźni zdradzają częściej typowe objawy tarczycy w przypadku zmęczenia i nadmiernego wysiłku.
Główne i najczęstsze choroby:
- Niedoczynność tarczycy;
- Wole guzkowe, rozsiane lub mieszane;
- Nowotwory złośliwe gruczołu.

Każda z tych chorób charakteryzuje się szczególnym obrazem klinicznym i etapami rozwoju.
Niedoczynność tarczycy
Jest to zespół przewlekłego zmniejszenia wydzielania T3 i T4, co pomaga spowolnić procesy metaboliczne organizm. Jednocześnie objawy choroby tarczycy mogą nie być odczuwalne przez długi czas, postępować powoli i maskować się jako inne choroby.
Niedoczynność tarczycy może być:
- Pierwotny - ze zmianami patologicznymi w tarczycy;
- Wtórne - ze zmianami w przysadce mózgowej;
- Trzeciorzędowy - ze zmianami w podwzgórzu.
Przyczynami choroby są:
- Zapalenie tarczycy, które występuje po zapaleniu tarczycy;
- zespół niedoboru jodu;
- Rehabilitacja po radioterapii;
- Okres pooperacyjny usuwania guzów, wola.

Objawy niedoczynności tarczycy są następujące:
- Powolne tętno, tętno;
- zawroty głowy;
- blada skóra;
- Dreszcze, drżenie;
- Wypadanie włosów, w tym brwi;
- Obrzęk twarzy, nóg, dłoni;
- Zmiany głosu, jego szorstkość;
- zaparcie;
- Zwiększenie wielkości wątroby;
- Przyrost masy ciała pomimo zmniejszonego apetytu;
- Utrata siły, bezwładność emocjonalna.
Leczenie niedoczynności tarczycy zwykle prowadzi się za pomocą leków hormonalnych, które kompensują brak hormonów tarczycy w organizmie. Należy jednak rozumieć, że takie leczenie jest wskazane w przypadku przewlekłym, który jest diagnozowany najczęściej. Jeśli choroba zostanie wykryta we wczesnym stadium, istnieje szansa na pobudzenie pracy organizmu poprzez wyeliminowanie przyczyn źródłowych i tymczasowe przyjęcie innej klasy hormonów.

Chorobę tę nazywa się chorobą damską, gdyż na dziesięciu pacjentek, u których zdiagnozowano nadczynność tarczycy, przypada dziewięć kobiet. Nadmierna produkcja hormonów prowadzi do przyspieszenia procesów metabolicznych, pobudzenia czynności serca, zaburzeń pracy ośrodkowego układu nerwowego i ANS. Wyraźne objawy choroby i zaawansowana postać nazywa się tyreotoksykozą.
Przyczyny rozwoju patologii:
- Zespół Gravesa-Basedowa, Plummera - wole o charakterze autoimmunologicznym lub wirusowym;
- Nowotwory złośliwe tarczycy lub przysadki mózgowej;
- Może rozwinąć się w wyniku długotrwałego leczenia lekami arytmicznymi.
Często choroba dotyka kobiety po rozpoczęciu menopauzy z powodu braku równowagi hormonalnej, a nie będącej konsekwencją nowotworów lub wola.
W tym przypadku główne objawy tarczycy u kobiet:
- przyspieszone bicie serca;
- Migotanie przedsionków;
- Wilgotność, gorąco skóry;
- drżenie palców;
- Drżenie może osiągnąć amplitudę, jak w chorobie Parkinsona;
- Podwyższona temperatura ciała, gorączka;
- zwiększone pocenie się;
- Biegunka ze zwiększonym apetytem;
- Zmniejszenie masy ciała;
- Zwiększenie wielkości wątroby;
- Drażliwość, drażliwość, bezsenność, niepokój.

Leczenie polega na przyjmowaniu tyreostatyków – leków zmniejszających aktywność wydzielania hormonów tarczycy. Tyreostatyki obejmują leki Tiamazol, Dijodotyrozyna, a także leki zapobiegające wchłanianiu jodu.
Ponadto zalecana jest specjalna dieta, w której wyklucza się alkohol, kawę, czekoladę, ostre przyprawy i przyprawy, które mogą pobudzać centralny układ nerwowy. Dodatkowo przepisywane są blokery adrenergiczne w celu ochrony mięśnia sercowego przed szkodliwym działaniem.
Choroba ma wyraźne objawy – już od drugiego stadium wola powiększa się gruczoł, co powoduje, że cała okolica szyi powyżej obojczyka, gdzie znajduje się tarczyca, nabiera zniekształconych konturów.
Wole może być guzkowe, rozlane i rozsiano-guzkowe. Przyczyny choroby są wystarczająco zróżnicowane - może to być brak jodu, zespół samorozwojowy i nadmierna ilość hormonów.
Objawy zależą od stopnia wola, którego w medycynie jest pięć:
- W pierwszym stopniu zwiększa się przesmyk gruczołu, co można wyczuć podczas połykania;
- Drugi stopień charakteryzuje się wzrostem zarówno cieśni, jak i bocznych płatów gruczołu, które są widoczne podczas połykania i dobrze wyczuwalne podczas badania palpacyjnego;
- W trzecim etapie gruczoł pokrywa całą ścianę szyi, zniekształcając jej kontury, widoczne gołym okiem;
- Czwarty stopień charakteryzuje się wyraźnie widocznym wolem, nawet wizualnie, zmianą kształtu szyi;
- Na stopień piąty wskazuje ogromne wole, które uciska tchawicę, naczynia krwionośne i zakończenia nerwowe szyi, powoduje kaszel, trudności w oddychaniu, połykaniu, szumy uszne, zaburzenia pamięci i snu.

charakterystyczne, ale niespecyficzny objaw Ta choroba tarczycy u kobiet to silne wysunięcie oczu, brak miesiączki do sześciu miesięcy lub dłużej, co często jest mylone z wczesną menopauzą.
Leczenie polega na terapia hormonalna na wczesnych etapach, na późniejszych etapach proponuje się interwencję chirurgiczną w celu usunięcia części narządu.
Ponadto leczenie zależy od rodzaju wola, ponieważ dzieli się na zespół Gravesa-Basedowa, wole eutyreotyczne, zespół Plummera i zespół Hashimoto. Precyzyjna definicja możliwe tylko przy kompleksowej diagnostyce.
Złośliwe formacje
Rozwijaj się na tle choroby przewlekłe tarczycy, które nie reagowały na leczenie. Wzrost komórek w gruczole może zostać sprowokowany i nieuprawniony.
Rokowanie jest pozytywne, ponieważ w większości przypadków jest diagnozowane wczesna faza i uleczalne. Czujność wymaga jedynie możliwych nawrotów.

Objawy:
- Ból w szyi;
- Foki, których dynamika wzrostu jest zauważalna nawet w ciągu dwóch tygodni;
- Ochrypły głos;
- trudności w oddychaniu;
- złe połykanie;
- Pocenie się, utrata masy ciała, osłabienie, słaby apetyt;
- Kaszel o charakterze niezakaźnym.
Wystarczy terminowa diagnoza terapia lekowa. W późniejszych etapach jest to pokazane usunięcie chirurgiczne.
Diagnostyka
Rozpoznanie jakiejkolwiek choroby tarczycy rozpoczyna się od zebrania wywiadu. Następnie przepisywane jest USG:
- Terminowe wykrywanie węzłów, cyst, nowotworów tarczycy;
- Określanie wielkości narządu;
- Diagnoza odchyleń od normy pod względem wielkości i objętości.

Diagnostyka laboratoryjna polega na analizie:
- AT-TPO;
- T3 – ogólny i bezpłatny;
- T4 - ogólny i bezpłatny;
- Markery nowotworowe w przypadku podejrzenia nowotworu;
- Ogólna analiza krwi i moczu.
W niektórych przypadkach można zalecić biopsję tkanek narządu w celu wyjaśnienia diagnozy, jeśli diagnostyka laboratoryjna nie wystarczyło. Nie zaleca się samodzielnej interpretacji wyników badań i stawiania diagnozy, ponieważ norma hormonów tarczycy jest inna dla każdej płci, wieku, choroby i wpływu chorób przewlekłych. Samoleczenie choroby autoimmunologiczne, a zwłaszcza onkologiczne, mogą zakończyć się zagrożeniem zdrowia i życia.
Jak bezpieczna jest operacja raka tarczycy?
 Leczenie przerostu tarczycy
Leczenie przerostu tarczycy
Co oznacza pojawienie się kaszlu z tarczycą?
 Cechy przebiegu autoimmunologicznego zapalenia tarczycy
Cechy przebiegu autoimmunologicznego zapalenia tarczycy
 Jak rozpoznać i leczyć torbiele tarczycy
Jak rozpoznać i leczyć torbiele tarczycy
 Przyczyny rozwoju gruczolaka w tarczycy
Przyczyny rozwoju gruczolaka w tarczycy
Tarczyca prawidłowa, a nawet bardziej patologicznie powiększona, jest zwykle łatwa do wyczucia palpacyjnego, co pozwala określić jej wielkość. W praktyczna praca masę tarczycy ocenia się na podstawie jej wielkości, ponieważ zarówno w normie, jak iw patologii istnieje zgodność między masą a wielkością tego gruczołu.
Palpacja prawidłowego gruczołu pozwala jednocześnie sprawdzić gładkość jego powierzchni i brak zagęszczenia, co przy rozmiarach odpowiadających wiekowi wskazuje na jego normalny stan.
A. V. Rumyantsev (N. A. Shereshevsky, O. L. Steppun i A. V. Rumyantsev, 1936) wskazuje, że w zarodku o długości 1,38 mm położenie tarczycy jest już wyraźnie widoczne mikroskopowo. W rezultacie w ludzkim zarodku zaczątki tarczycy pojawiają się bardzo wcześnie. Patten (1959) i kilku innych autorów szczegółowo opisuje rozwój tarczycy w zarodku ludzkim.
Po powstaniu tarczycy, co następuje nawet w okresie prenatalnym, gruczoł ten charakteryzuje się tym cechy zewnętrzne, czyli formę i liczbę akcji obserwowaną we wszystkich kolejnych latach.
Jak wiadomo, tarczyca jest narządem w kształcie podkowy, składającym się z 2 płatów bocznych (prawego i lewego), połączonych u dołu wąską środkową częścią, przesmykiem (isthmus Breastulae thyreoideae). Czasami (według niektórych danych nawet u 30%) przesmyk ten jest całkowicie nieobecny, co najwyraźniej nie jest związane z odchyleniami w funkcji tego ważny gruczoł z wydzieliną wewnętrzną.
Oba boczne płaty tego narządu w kształcie podkowy, znajdujące się z przodu szyi, są skierowane do góry.
Wymiary płatów bocznych tarczycy charakteryzują się znaczną zmiennością osobniczą. Odpowiednie dane dotyczące wielkości podane w różnych wytycznych różnią się nawet wtedy, gdy odnoszą się do tego samego wieku i tej samej płci, przy tej samej masie całkowitej osoby badanej.
Podręcznik anatomii Rauber-Kopsch (1911) wskazuje, że każdy z bocznych płatów tego gruczołu u osoby dorosłej ma długość od 5 do 8 cm i szerokość od 3 do 4 cm, a grubość środka gruczołu wynosi od 1,5 do 2,5 cm Długość i szerokość prawego i lewego płata nie zawsze są takie same, prawy jest często większy.
Rozmiar i kształt przesmyku łączącego oba płaty są bardzo zróżnicowane. Jego szerokość wynosi najczęściej 1,5-2 cm, a grubość 0,5-1,5 cm Tylna powierzchnia cieśni przylega do drugiego i trzeciego pierścienia tchawicy, a czasami do pierwszego pierścienia.
Od przesmyku w górę do kości gnykowej odchodzi występ tarczycy - tak zwany płat piramidalny (lub proces piramidalny). Czasami odchodzi nie od części środkowej, ale z boku, w tych przypadkach częściej od lewej (Rauber-Kopsch). Jeśli przesmyk jest nieobecny, wówczas oczywiście nie ma płata piramidowego.
Średnia masa tarczycy u noworodka wynosi 1,9 g, u 1-latka – 2,5 g, u 5-latka – 6 g, u 10-latka – 8,7 g, u 15-latka -latek - 15,8 g, dorosły - 20 g (wg Salzer'a).
Wohefritz (wg Neuratha, 1932) wskazuje, że masa tarczycy w wieku 5 lat wynosi średnio 4,39 g, w wieku 10 lat - 7,65 g, w wieku 20 lat - 18,62 g i w wieku 30 lat - 27 g. dla organizmu w okresie wzrostu, podaje się te same dane dotyczące średniej masy, jakie wskazał Salzer.
Według Neuratha stosunek masy tarczycy do masy ciała jest następujący. U noworodka 1:400, a nawet 1:243, u trzytygodniowego - 1:1166, u dorosłego - 1:1800. Dane te pokazują, jak stosunkowo duża jest masa tarczycy u noworodka. Ten wzór jest jeszcze bardziej wyraźny w okresie prenatalnym. Ponadto wszyscy badacze podkreślają, że u kobiet masa tarczycy jest większa niż u mężczyzn. Już w okresie prenatalnym masa tego gruczołu u zarodków żeńskich jest większa niż u zarodków męskich (Neurath).
Wegelin (wg Neuratha) podaje następujące średnie wartości masy tarczycy w różnych przedziałach wiekowych: 1 – 10 dni życia – 1,9 g, 1 rok – 2,4 g, 2 lata – 3,73 g, 3 lata – 6,1 g , 4 lata – 6,12 g, 5 lat – 8,6 g, 11-15 lat – 11,2 g, 16-20 lat – 22 g, 21-30 lat – 23,5 g, 31-40 lat – 24 g , 41-50 lat - 25,3 g, 51-70 lat - 19-20 lat W rezultacie w starszym wieku masa tego gruczołu już spada.
U osób wysokich masa tarczycy jest nieco większa niż u osób niższego wzrostu (wg Neuratha).
Niezwykle rzadko obserwuje się dystopię, czyli przemieszczenie części podstawy tarczycy w nietypowe miejsce. Czasami jeden płat lub nawet cały gruczoł tarczycy zostaje przemieszczony do śródpiersia. Czasami taką dystopię stwierdza się w obszarze rozwoju przyszłej kończyny. Taki zarodek, jak również całkowicie lub częściowo uformowany niezwykłe miejsce tarczyca może nadal funkcjonować w sposób charakterystyczny dla tarczycy.
Niemniej jednak element o nieprawidłowej lokalizacji może zamienić tę lub inną długość w część tarczycy dotkniętą rakiem, ze wszystkimi strasznymi konsekwencjami tego złośliwego nowotworu. Znajduje się to w różne daty czasami po latach lub dekadach.
Różnice indywidualne w masie i wielkości tarczycy występują we wszystkich przedziałach wiekowych.
Indywidualne cechy funkcjonalne normalnej tarczycy są również dość wyraźnie wyrażone we wszystkich przedziałach wiekowych.
Granice normy i „jeszcze normalnej” pod względem wielkości i wagi są bardzo szerokie. Wydają się większe niż we wszystkich innych gruczołach dokrewnych.
Składa się z dwóch płatów i przesmyku i znajduje się przed krtanią. Masa tarczycy wynosi 30 g.
Główną jednostką strukturalną i funkcjonalną gruczołu są pęcherzyki - zaokrąglone wnęki, których ścianę tworzy jeden rząd prostopadłościennych komórek nabłonka. Mieszki są wypełnione koloidem i zawierają hormony tyroksyna I trójjodotyronina związany z białkiem tyreoglobuliny. W przestrzeni międzypęcherzykowej znajdują się komórki C wytwarzające hormon tyrokalcytonina. Gruczoł jest bogato uzbrojony w naczynia krwionośne i limfatyczne. Ilość przepływająca przez tarczycę w ciągu 1 minuty jest 3-7 razy większa niż masa samego gruczołu.
Biosynteza tyroksyny i trójjodotyroniny Odbywa się to w wyniku jodowania aminokwasu tyrozyny, dlatego aktywne wchłanianie jodu zachodzi w tarczycy. Zawartość jodu w pęcherzykach jest 30 razy wyższa niż jego stężenie we krwi, a przy nadczynności tarczycy stosunek ten staje się jeszcze większy. Wchłanianie jodu odbywa się w wyniku transportu aktywnego. Po połączeniu tyrozyny wchodzącej w skład tyreoglobuliny z jodem atomowym powstają monojodotyrozyna i dijodotyrozyna. W wyniku połączenia dwóch cząsteczek dijodotyrozyny powstaje tetrajodotyronina, czyli tyroksyna; kondensacja mono- i dijodotyrozyny prowadzi do powstania trójjodotyroniny. Następnie w wyniku działania proteaz rozkładających tyreoglobulinę do krwi uwalniane są aktywne hormony.
Aktywność tyroksyny jest kilkakrotnie mniejsza niż trójjodotyroniny, ale zawartość tyroksyny we krwi jest około 20 razy większa niż trójjodotyroniny. Tyroksynę można dejodować do trójjodotyroniny. Na podstawie tych faktów przyjmuje się, że głównym hormonem tarczycy jest trójjodotyronina, a tyroksyna pełni funkcję jej prekursora.
Synteza hormonów jest nierozerwalnie związana z przyjmowaniem jodu przez organizm. Jeśli w regionie zamieszkania jodu brakuje w wodzie i glebie, brakuje go także w produktach spożywczych pochodzenia roślinnego i zwierzęcego. W tym przypadku, aby zapewnić wystarczającą syntezę hormonu, tarczyca u dzieci i dorosłych zwiększa się, czasami bardzo znacząco, tj. występuje wole. Nazywa się to wzrostem nie tylko kompensacyjnym, ale także patologicznym wole endemiczne. Brak jodu w diecie najlepiej rekompensują wodorosty i inne owoce morza, sól jodowana, woda mineralna stołowa zawierająca jod, pieczywo z suplementami jodu. Jednak nadmierne spożycie jodu w organizmie powoduje obciążenie tarczycy i może prowadzić do poważnych konsekwencji.
Hormony tarczycy

Działanie tyroksyny i trójjodotyroniny
Podstawowy:
- aktywują aparat genetyczny komórki, stymulują metabolizm, zużycie tlenu i intensywność procesów oksydacyjnych
Metaboliczny:
- metabolizm białek: stymulują syntezę białek, ale w przypadku, gdy poziom hormonów przekracza normę, dominuje katabolizm;
- metabolizm tłuszczów: stymulują lipolizę;
- metabolizm węglowodanów: w czasie nadprodukcji następuje pobudzenie glikogenolizy, wzrost poziomu glukozy we krwi, aktywacja jej wnikania do komórek oraz aktywacja insulinazy wątrobowej
Funkcjonalny:
- zapewniają rozwój i różnicowanie tkanek, zwłaszcza nerwowych;
- wzmacniają działanie współczulnego układu nerwowego poprzez zwiększenie liczby adrenoreceptorów i hamowanie monoaminooksydazy;
- działanie prosympatyczne objawia się wzrostem częstości akcji serca, objętości skurczowej, ciśnienia krwi, częstości oddechów, motoryki jelit, pobudliwości OUN, podwyższonej temperatury ciała
Manifestacje zmian w produkcji tyroksyny i trójjodotyroniny
Charakterystyka porównawcza niedostatecznej produkcji somatotropiny i tyroksyny
Wpływ hormonów tarczycy na funkcje organizmu
Charakterystycznym działaniem hormonów tarczycy (tyroksyny i trójjodotyroniny) jest zwiększenie metabolizmu energetycznego. Wprowadzeniu zawsze towarzyszy wzrost zużycia tlenu, a usunięciu tarczycy towarzyszy jej zmniejszenie. Wraz z wprowadzeniem hormonu zwiększa się metabolizm, zwiększa się ilość uwalnianej energii i wzrasta temperatura ciała.
Tyroksyna zwiększa wydatek. Następuje utrata masy ciała i intensywne zużycie glukozy z krwi przez tkanki. Spadek poziomu glukozy we krwi jest kompensowany przez jej uzupełnienie w wyniku zwiększonego rozkładu glikogenu w wątrobie i mięśniach. Zmniejszają się zapasy lipidów w wątrobie, zmniejsza się ilość cholesterolu we krwi. Zwiększa się wydalanie wody, wapnia i fosforu z organizmu.
Hormony tarczycy powodują zwiększoną pobudliwość, drażliwość, bezsenność, brak równowagi emocjonalnej.
Tyroksyna zwiększa minimalną objętość krwi i częstość akcji serca. Hormon tarczycy jest niezbędny do owulacji, pomaga w utrzymaniu ciąży, reguluje pracę gruczołów sutkowych.
Wzrost i rozwój organizmu reguluje także tarczyca: osłabienie jej funkcji powoduje zatrzymanie wzrostu. Hormon tarczycy pobudza hematopoezę, zwiększa wydzielanie żołądka, jelit i wydzielanie mleka.
Oprócz hormonów zawierających jod, tarczyca produkuje tyrokalcytonina, zmniejszenie ilości wapnia we krwi. Tyrokalcytonina jest antagonistą hormonu przytarczyc. Tyrokalcytonina działa na tkankę kostną, wzmaga aktywność osteoblastów i proces mineralizacji. W nerkach i jelitach hormon hamuje wchłanianie zwrotne wapnia i pobudza ssanie wsteczne fosforany. Realizacja tych efektów prowadzi do hipokalcemia.
Nadczynność i niedoczynność gruczołu
nadczynność (nadczynność tarczycy) powoduje chorobę zwaną Choroba Gravesa. Główne objawy choroby: wole, wyłupiaste oczy, zwiększony metabolizm, tętno, wzmożona potliwość, aktywność silnika(kłopotliwość), drażliwość (kapryśność, gwałtowne zmiany nastroju, niestabilność emocjonalna), szybkie męczenie się. Wole powstaje w wyniku rozlanego powiększenia tarczycy. Obecnie metody leczenia są na tyle skuteczne, że ciężkie przypadki choroby zdarzają się dość rzadko.
Niedoczynność (niedoczynność tarczycy) tarczyca, która pojawia się w młodym wieku, do 3-4 lat, powoduje rozwój objawów kretynizm. Dzieci cierpiące na kretynizm są opóźnione w rozwoju fizycznym i psychicznym. Objawy choroby: karłowaty wzrost i naruszenie proporcji ciała, szeroki, głęboko zapadnięty grzbiet nosa, szeroko rozstawione oczy, otwarte usta i stale wystający język, ponieważ nie dostaje się do ust, krótki i zakrzywione kończyny, tępy wyraz twarzy. Średnia długość życia takich osób zwykle nie przekracza 30-40 lat. W ciągu pierwszych 2-3 miesięcy życia można osiągnąć późniejszą normalność rozwój mentalny. Jeśli leczenie rozpocznie się w wieku jednego roku, wówczas 40% dzieci, które przeszły tę chorobę, pozostaje na bardzo niskim poziomie rozwoju umysłowego.
Niedoczynność tarczycy u dorosłych prowadzi do choroby zwanej obrzęk śluzowy, Lub obrzęk śluzowy. W przypadku tej choroby zmniejsza się intensywność procesów metabolicznych (o 15-40%), temperatura ciała, tętno staje się rzadsze, spada ciśnienie krwi, pojawia się obrzęk, wypadają włosy, łamią się paznokcie, twarz staje się blada, pozbawiona życia, maska- tak jak. Pacjenci charakteryzują się spowolnieniem, sennością, słabą pamięcią. Obrzęk śluzowaty jest powoli postępującą chorobą, która nieleczona prowadzi do całkowitej niepełnosprawności.
Regulacja funkcji tarczycy
Specyficznym regulatorem pracy tarczycy jest jod, sam hormon tarczycy oraz TSH (hormon tyreotropowy). Jod w małych dawkach zwiększa wydzielanie TSH, a w dużych je hamuje. Tarczyca znajduje się pod kontrolą centralnego układu nerwowego. Taki produkty żywieniowe podobnie jak kapusta, rutabaga, rzepa, hamują pracę tarczycy. Produkcja tyroksyny i trójjodotyroniny gwałtownie wzrasta w warunkach długotrwałego działania pobudzenie emocjonalne. Należy również zauważyć, że wydzielanie tych hormonów przyspiesza wraz ze spadkiem temperatury ciała.
Objawy zaburzeń funkcji hormonalnej tarczycy
Wraz ze wzrostem aktywności funkcjonalnej tarczycy i nadmierną produkcją hormonów tarczycy pojawia się stan nadczynność tarczycy (nadczynność tarczycy)), charakteryzujący się wzrostem poziomu hormonów tarczycy we krwi. Objawy tego stanu można wytłumaczyć działaniem hormonów tarczycy podwyższone stężenia. Tak więc, ze względu na wzrost podstawowego metabolizmu (hipermetabolizmu), pacjenci doświadczają niewielki wzrost temperatura ciała (hipertermia). Zmniejszenie masy ciała pomimo zaoszczędzonej lub zwiększony apetyt. Stan ten objawia się wzrostem zapotrzebowania na tlen, tachykardią, wzrostem kurczliwości mięśnia sercowego, wzrostem skurczowego ciśnienia krwi i wzrostem wentylacji płuc. Zwiększa się aktywność ATP, zwiększa się liczba receptorów p-adrenergicznych, rozwija się pocenie się, nietolerancja ciepła. Zwiększa się pobudliwość i labilność emocjonalna, mogą pojawić się drżenie kończyn i inne zmiany w organizmie.
Wzmożone wytwarzanie i wydzielanie hormonów tarczycy może wynikać z szeregu czynników, których prawidłowa identyfikacja decyduje o wyborze metody korekcji czynności tarczycy. Wśród nich znajdują się czynniki powodujące nadczynność komórek pęcherzykowych tarczycy (guzy gruczołu, mutacje białek G) oraz wzrost tworzenia i wydzielania hormonów tarczycy. Nadczynność tyreocytów obserwuje się przy nadmiernej stymulacji receptorów tyreotropiny przez zwiększoną zawartość TSH, na przykład w guzach przysadki mózgowej lub zmniejszoną wrażliwość receptorów hormonów tarczycy w tyreotrofiach przysadki mózgowej. popularny przypadek nadczynność tyreocytów, zwiększenie wielkości gruczołu, to pobudzenie receptorów TSH przez wytwarzane przeciwko nim przeciwciała w chorobie autoimmunologicznej zwanej chorobą Gravesa-Basedowa (ryc. 1). Przejściowy wzrost poziomu hormonów tarczycy we krwi może rozwinąć się wraz z zniszczeniem tyreocytów na skutek procesów zapalnych w gruczole (toksyczne zapalenie tarczycy Hashimoto), przyjmowania nadmiernej ilości hormonów tarczycy i preparatów jodu.
Może wystąpić podwyższony poziom hormonów tarczycy tyreotoksykoza; w tym przypadku mówi się o nadczynności tarczycy z tyreotoksykozą. Ale tyreotoksykoza może rozwinąć się, gdy do organizmu zostanie wprowadzona nadmierna ilość hormonów tarczycy, przy braku nadczynności tarczycy. Opisano rozwój tyreotoksykozy na skutek zwiększonej wrażliwości receptorów komórkowych na hormony tarczycy. Zdarzają się także przypadki odwrotne, gdy zmniejsza się wrażliwość komórek na hormony tarczycy i rozwija się stan oporności na hormony tarczycy.
Zmniejszone wytwarzanie i wydzielanie hormonów tarczycy może być spowodowane wieloma przyczynami, a niektóre z nich są wynikiem naruszenia mechanizmów regulacji funkcji tarczycy. Więc, niedoczynność tarczycy (niedoczynność tarczycy) może rozwijać się wraz ze zmniejszeniem tworzenia TRH w podwzgórzu (guzy, cysty, promieniowanie, zapalenie mózgu w podwzgórzu itp.). Ta niedoczynność tarczycy nazywana jest trzeciorzędową. Wtórna niedoczynność tarczycy rozwija się z powodu niewystarczającego wytwarzania THG przez przysadkę mózgową (guzy, torbiele, promieniowanie, chirurgiczne usunięcie części przysadki mózgowej, zapalenie mózgu itp.). Pierwotna niedoczynność tarczycy może rozwinąć się w wyniku autoimmunologicznego zapalenia gruczołu, przy niedoborze jodu, selenu, nadmiernym przyjmowaniu produktów goitrogennych – goitrogenów (niektóre odmiany kapusty), po naświetlaniu gruczołu, długotrwałym stosowaniu szeregu leków leki (jod, lit, leki przeciwtarczycowe) itp.

Ryż. 1. Rozlane powiększenie tarczycy u 12-letniej dziewczynki z autoimmunologicznym zapaleniem tarczycy (T. Foley, 2002)
Niedostateczna produkcja hormonów tarczycy prowadzi do zmniejszenia intensywności metabolizmu, zużycia tlenu, wentylacji, kurczliwości mięśnia sercowego i minimalnej objętości krwi. W ciężkiej niedoczynności tarczycy występuje stan tzw obrzęk śluzowy- obrzęk śluzowy. Rozwija się na skutek gromadzenia się (prawdopodobnie pod wpływem podwyższonego poziomu TSH) mukopolisacharydów i wody w podstawnych warstwach skóry, co prowadzi do obrzęków twarzy i lepkości skóry, a także przyrostu masy ciała pomimo zmniejszenia apetytu. U pacjentów z obrzękiem śluzowym może wystąpić opóźnienie umysłowe i motoryczne, senność, dreszcze, obniżona inteligencja i napięcie sympatyczny dział ANS i inne zmiany.
W realizację złożonych procesów powstawania hormonów tarczycy zaangażowane są pompy jonowe, które zapewniają dostawę jodu, szeregu enzymów o charakterze białkowym, wśród których kluczową rolę odgrywa tyreoperoksydaza. W niektórych przypadkach dana osoba może mieć wadę genetyczną prowadzącą do naruszenia jej struktury i funkcji, czemu towarzyszy naruszenie syntezy hormonów tarczycy. Można zaobserwować defekty genetyczne w budowie tyreoglobuliny. Często wytwarzane są autoprzeciwciała przeciwko tyropoksydazie i tyreoglobulinie, czemu towarzyszy również naruszenie syntezy hormonów tarczycy. Na aktywność procesów wychwytu jodu i jego włączania do tyreoglobuliny może wpływać szereg czynników: środki farmakologiczne poprzez regulację syntezy hormonów. Na ich syntezę można wpływać poprzez przyjmowanie preparatów jodu.
Rozwój niedoczynności tarczycy u płodu i noworodka może prowadzić do pojawienia się kretynizm - fizyczne (niski wzrost, naruszenie proporcji ciała), niedorozwój seksualny i psychiczny. Zmianom tym można zapobiec poprzez odpowiednią terapię zastępczą hormonami tarczycy w pierwszych miesiącach po urodzeniu dziecka.
Struktura tarczycy
Jest to największy narząd wydzielania wewnętrznego pod względem masy i wielkości. Zwykle składa się z dwóch płatów, połączonych przesmykiem i znajduje się na przedniej powierzchni szyi, i jest przymocowany tkanką łączną do przedniej i bocznej powierzchni tchawicy i krtani. Średnia masa prawidłowej tarczycy u dorosłych waha się w granicach 15-30 g, jednak jej wielkość, kształt i topografia lokalizacji są bardzo zróżnicowane.
Czynnie czynna tarczyca jest pierwszym z gruczołów wydzielania wewnętrznego, który pojawia się w procesie embriogenezy. Układanie tarczycy u płodu ludzkiego powstaje w 16-17 dniu rozwoju wewnątrzmacicznego w postaci nagromadzenia komórek endodermalnych u nasady języka.
We wczesnych stadiach rozwoju (6-8 tygodni) podstawą gruczołu jest warstwa intensywnie proliferującego komórki nabłonkowe. W tym okresie gruczoł rośnie szybko, ale nie powstają jeszcze w nim hormony. Pierwsze oznaki ich wydzielania wykrywa się po 10-11 tygodniach (u płodów o wielkości około 7 cm), kiedy komórki gruczołów są już w stanie wchłonąć jod, utworzyć koloid i syntetyzować tyroksynę.
Pod torebką pojawiają się pojedyncze pęcherzyki, w których tworzą się komórki pęcherzykowe.
Komórki parafolikularne (prawie pęcherzykowe) lub C wyrastają z podstawy tarczycy z piątej pary kieszeni skrzelowych. W 12-14 tygodniu rozwoju płodu cały prawy płat tarczycy nabiera struktury pęcherzykowej, a lewy dwa tygodnie później. W 16-17 tygodniu tarczyca płodu jest już w pełni zróżnicowana. Gruczoły tarczowe płodów w wieku 21–32 tygodni charakteryzują się wysoką aktywnością funkcjonalną, która utrzymuje się do 33–35 tygodnia.

W miąższu gruczołu wyróżnia się trzy typy komórek: A, B i C. Większość komórek miąższu stanowią tyreocyty (komórki pęcherzykowe lub A). Wyścielają ścianę mieszków włosowych, w których jamach znajduje się koloid. Każdy pęcherzyk otoczony jest gęstą siecią naczyń włosowatych, do światła którego wchłaniana jest wydzielana przez tarczycę tyroksyna i trójjodotyronina.
W niezmienionej tarczycy pęcherzyki są równomiernie rozmieszczone w miąższu. Przy niskiej aktywności funkcjonalnej gruczołu tyreocyty są zwykle płaskie, przy wysokiej - cylindryczne (wysokość komórek jest proporcjonalna do stopnia aktywności prowadzonych w nich procesów). Koloid wypełniający szczeliny mieszków włosowych jest jednorodną lepką cieczą. Większość koloidu stanowi tyreoglobulina wydzielana przez tyreocyty do światła pęcherzyka.
Limfocyty B (komórki Ashkenazi-Gurtla) są większe od tyreocytów, mają eozynofilową cytoplazmę i zaokrąglone, centralnie położone jądro. W cytoplazmie tych komórek znaleziono aminy biogenne, w tym serotoninę. Po raz pierwszy komórki B pojawiają się w wieku 14-16 lat. W dużych ilościach spotykane są u osób w wieku 50-60 lat.
Komórki parafolikularne, czyli komórki C (w rosyjskiej transkrypcji komórek K), różnią się od tyreocytów brakiem zdolności do wchłaniania jodu. Zapewniają syntezę kalcytoniny, hormonu biorącego udział w regulacji metabolizmu wapnia w organizmie. Komórki C są większe niż tyreocyty, z reguły znajdują się pojedynczo w składzie pęcherzyków. Ich morfologia jest typowa dla komórek syntetyzujących białka na eksport (występuje szorstka siateczka śródplazmatyczna, kompleks Golgiego, ziarnistości wydzielnicze, mitochondria). W preparatach histologicznych cytoplazma komórek C wygląda jaśniej niż cytoplazma tyreocytów, stąd ich nazwa - komórki lekkie.
Jeśli na poziomie tkanki główną jednostką strukturalną i funkcjonalną tarczycy są pęcherzyki otoczone błonami podstawnymi, wówczas jedną z proponowanych jednostek narządów tarczycy mogą być mikrozraziki, które obejmują pęcherzyki, komórki C, hemokapilary, bazofile tkankowe. Skład mikrolobule obejmuje 4-6 pęcherzyków otoczonych błoną fibroblastów.
Do chwili urodzenia tarczyca jest już funkcjonalnie aktywna i strukturalnie całkowicie zróżnicowana. U noworodków pęcherzyki w miarę rozwoju są małe (o średnicy 60–70 mikronów). ciało dziecka ich rozmiar wzrasta i u dorosłych osiąga 250 mikronów. Przez pierwsze dwa tygodnie po urodzeniu pęcherzyki rozwijają się intensywnie, po 6 miesiącach są już dobrze rozwinięte w całym gruczole, a po roku osiągają średnicę 100 mikronów. W okresie dojrzewania następuje wzrost miąższu i zrębu gruczołu, wzrost jego aktywności funkcjonalnej, objawiający się wzrostem wysokości tyreocytów, wzrostem aktywności w nich enzymów.
U osoby dorosłej tarczyca przylega do krtani i górnej części tchawicy w taki sposób, że cieśń znajduje się na poziomie półpierścieni tchawicy II-IV.
Masa i wielkość tarczycy zmieniają się przez całe życie. Na zdrowy noworodek masa gruczołu waha się od 1,5 do 2 g. Pod koniec pierwszego roku życia masa podwaja się i powoli wzrasta w okresie dojrzewania do 10–14 g. Wzrost masy jest szczególnie zauważalny w wieku od 5–7 lat. Masa tarczycy w wieku 20-60 lat waha się od 17 do 40 g.
Tarczyca ma wyjątkowo obfite ukrwienie w porównaniu do innych narządów. Objętościowe natężenie przepływu krwi w tarczycy wynosi około 5 ml/g na minutę.
Tarczyca jest zaopatrywana w krew przez parę tętnic tarczowych górnych i dolnych. Czasami niesparowana, najniższa tętnica (a. tarczycaja).
Odpływ krwi żylnej z tarczycy odbywa się przez żyły tworzące sploty na obwodzie płatów bocznych i przesmyku. Tarczyca posiada rozbudowaną sieć naczyń limfatycznych, poprzez które limfa dociera do głębokich węzłów chłonnych szyjnych, następnie do nadobojczykowych i bocznych głębokich węzłów chłonnych szyjnych. Odprowadzające naczynia limfatyczne bocznych szyjnych węzłów chłonnych głębokich tworzą po obu stronach szyi pień szyjny, który uchodzi do przewodu piersiowego po lewej stronie i do prawego przewodu limfatycznego po prawej stronie.
Tarczyca jest unerwiona przez włókna pozazwojowe współczulnego układu nerwowego z górnych, środkowych (głównie) i dolnych węzłów szyjnych pnia współczulnego. Nerwy tarczycy tworzą sploty wokół naczyń prowadzących do gruczołu. Uważa się, że nerwy te pełnią funkcję naczynioruchową. Nerw błędny bierze również udział w unerwieniu tarczycy, przenosząc włókna przywspółczulne do gruczołu jako część górnego i dolnego nerwu krtaniowego. Synteza zawierających jod hormonów tarczycy T 3 i T 4 odbywa się przez pęcherzykowe komórki A - tyreocyty. Hormony T3 i T4 są jodowane.
Hormony T4 i T3 są jodowanymi pochodnymi aminokwasu L-tyrozyny. Jod, będący częścią ich struktury, stanowi 59-65% masy cząsteczki hormonu. Zapotrzebowanie jodu do prawidłowej syntezy hormonów tarczycy przedstawiono w tabeli. 1. Kolejność procesów syntezy upraszcza się w następujący sposób. Jod w postaci jodku pobierany jest z krwi za pomocą pompy jonowej, gromadzi się w tyreocytach, ulega utlenieniu i zostaje włączony do pierścienia fenolowego tyrozyny jako część tyreoglobuliny (organizacji jodowej). Jodowanie tyreoglobuliny z utworzeniem mono- i dijodotyrozyny zachodzi na granicy tyreocytu i koloidu. Następnie przeprowadza się połączenie (kondensację) dwóch cząsteczek dijodotyrozyny z utworzeniem T 4 lub dijodotyrozyny i monojodotyrozyny z utworzeniem T 3 . Część tyroksyny ulega odjodowaniu w tarczycy, tworząc trójjodotyroninę.
Tabela 1. Normy spożycia jodu (WHO, 2005. by I. Dedov i in. 2007)
Jodowana tyreoglobulina wraz z przyłączonymi do niej T4 i T3 gromadzi się i magazynuje w pęcherzykach w postaci koloidu, pełniąc funkcję magazynu hormonów tarczycy. Uwalnianie hormonów następuje w wyniku pinocytozy koloidu pęcherzykowego i późniejszej hydrolizy tyreoglobuliny w fagolizosomach. Uwolnione T4 i T3 są wydzielane do krwi.
Podstawowe dzienne wydzielanie przez tarczycę wynosi około 80 µg T 4 i 4 µg T 3. Jednocześnie tyreocyty pęcherzyków tarczycy są jedynym źródłem endogennego tworzenia T 4. W przeciwieństwie do T 4 , T 3 powstaje w tyreocytach w niewielkiej ilości, a główne tworzenie tej aktywnej formy hormonu odbywa się w komórkach wszystkich tkanek organizmu poprzez odjodowanie około 80% T 4 .
Zatem oprócz gruczołowego magazynu hormonów tarczycy w organizmie znajduje się drugi - pozagruczołowy magazyn hormonów tarczycy, reprezentowany przez hormony związane z białkami transportującymi krew. Rolą tych magazynów jest zapobieganie szybkiemu spadkowi poziomu hormonów tarczycy w organizmie, które mogłoby nastąpić przy krótkotrwałym zmniejszeniu ich syntezy, np. przy krótkotrwałym zmniejszeniu spożycia jodu. Związana forma hormonów we krwi uniemożliwia ich szybkie wydalanie z organizmu przez nerki, chroni komórki przed niekontrolowanym przyjmowaniem hormonów. Wolne hormony dostają się do komórek w ilościach proporcjonalnych do ich potrzeb funkcjonalnych.
Tyroksyna wnikając do komórek ulega dejodowaniu pod wpływem enzymów dejodynazy, a po odszczepieniu jednego atomu jodu powstaje z niej bardziej aktywny hormon – trójjodotyronina. W tym przypadku, w zależności od dróg odjodowania, z T4 może powstać zarówno aktywny T3, jak i nieaktywny odwrotny T3 (3,3,5"-trijod-L-tyronina - pT3). Hormony te przekształcają się poprzez kolejne odjodowanie w metabolity T 2 , następnie T 1 i T 0 , które są sprzęgane z kwasem glukuronowym lub siarczanem w wątrobie i wydalane z żółcią i przez nerki z organizmu. Aktywność biologiczną może wykazywać nie tylko T3, ale także inne metabolity tyroksyny.
Mechanizm działania hormonów tarczycy wynika przede wszystkim z ich interakcji z receptorami jądrowymi, które są białkami niehistonowymi, zlokalizowanymi bezpośrednio w jądrze komórkowym. Istnieją trzy główne podtypy receptorów hormonów tarczycy: TPβ-2, TPβ-1 i TPa-1. W wyniku interakcji z T3 następuje aktywacja receptora, kompleks hormon-receptor oddziałuje z wrażliwym na hormony regionem DNA i reguluje aktywność transkrypcyjną genów.
Odkryto szereg niegenomowych skutków działania hormonów tarczycy na mitochondria, czyli błonę komórkową komórek. W szczególności hormony tarczycy mogą zmieniać przepuszczalność błon mitochondrialnych dla protonów wodoru, a poprzez rozłączenie procesów oddychania i fosforylacji zmniejszać syntezę ATP i zwiększać wytwarzanie ciepła w organizmie. Zmieniają przepuszczalność błony plazmatyczne dla jonów Ca 2+ i wpływają na wiele procesów wewnątrzkomórkowych realizowanych z udziałem wapnia.
Główne skutki i rola hormonów tarczycy
Możliwe jest normalne funkcjonowanie wszystkich narządów i tkanek organizmu bez wyjątku normalny poziom hormony tarczycy, ponieważ wpływają na wzrost i dojrzewanie tkanek, metabolizm energetyczny oraz metabolizm białek, lipidów, węglowodanów, kwasów nukleinowych, witamin i innych substancji. Przydziel metaboliczne i inne skutki fizjologiczne hormony tarczycy.
Efekty metaboliczne:
- aktywacja procesów oksydacyjnych i wzrost podstawowej przemiany materii, zwiększony pobór tlenu przez tkanki, zwiększone wytwarzanie ciepła i temperatura ciała;
- stymulacja syntezy białek (działanie anaboliczne) w stężeniach fizjologicznych;
- zwiększone utlenianie Kwasy tłuszczowe i spadek ich poziomu we krwi;
- hiperglikemia spowodowana aktywacją glikogenolizy w wątrobie.
Efekty fizjologiczne:
- zapewnienie prawidłowych procesów wzrostu, rozwoju, różnicowania komórek, tkanek i narządów, w tym ośrodkowego układu nerwowego (mielinizacja włókien nerwowych, różnicowanie neuronów), a także procesów fizjologicznej regeneracji tkanek;
- wzmocnienie działania SNS poprzez zwiększoną wrażliwość receptorów adrenergicznych na działanie Adr i NA;
- zwiększona pobudliwość ośrodkowego układu nerwowego i aktywacja procesów mentalnych;
- udział w zapewnieniu funkcji rozrodczych (przyczyniają się do syntezy GH, FSH, LH i realizacji działania insulinopodobnego czynnika wzrostu – IGF);
- udział w tworzeniu reakcji adaptacyjnych organizmu na niekorzystne skutki, w szczególności zimno;
- udział w rozwoju układu mięśniowego, zwiększając siłę i szybkość skurczu mięśni.
Tworzenie, wydzielanie i transformacja hormonów tarczycy są regulowane przez złożone mechanizmy hormonalne, nerwowe i inne. Ich wiedza pozwala zdiagnozować przyczyny zmniejszenia lub zwiększenia wydzielania hormonów tarczycy.
W regulacji wydzielania hormonów tarczycy kluczową rolę odgrywają hormony osi podwzgórze-przysadka-tarczyca (ryc. 2). Podstawowe wydzielanie hormonów tarczycy i jego zmiany pod różnymi wpływami regulowane są przez poziom TRH podwzgórza i TSH przysadki mózgowej. TRH stymuluje produkcję TSH, co ma stymulujący wpływ na prawie wszystkie procesy zachodzące w tarczycy oraz wydzielanie T 4 i T 3 . W normalnym warunki fizjologiczne powstawanie TRH i TSH jest kontrolowane przez poziom wolnego T 4 i T. we krwi w oparciu o mechanizmy negatywne informacja zwrotna. Jednocześnie wydzielanie TRH i TSH jest hamowane przez wysoki poziom hormonów tarczycy we krwi, a przy ich niskim stężeniu wzrasta.

Ryż. Ryc. 2. Schematyczne przedstawienie regulacji powstawania i wydzielania hormonów w osi podwzgórze – przysadka mózgowa – tarczyca
Duże znaczenie w mechanizmach regulacji hormonów osi podwzgórze-przysadka-tarczyca ma stan wrażliwości receptorów na działanie hormonów na różnych poziomach tej osi. Zmiany w strukturze tych receptorów lub ich pobudzenie przez autoprzeciwciała mogą być przyczyną upośledzenia produkcji hormonów tarczycy.
Tworzenie się hormonów w samym gruczole zależy od otrzymania wystarczającej ilości jodku z krwi - 1-2 mikrogramów na 1 kg masy ciała (patrz ryc. 2).
Przy niewystarczającym spożyciu jodu w organizmie rozwijają się w nim procesy adaptacyjne, które mają na celu najbardziej ostrożny i efektywne wykorzystanie zawarty w nim jod. Polegają one na zwiększonym przepływie krwi przez gruczoł, skuteczniejszym pobieraniu jodu przez tarczycę z krwi, zmianach w procesach syntezy hormonów i wydzielaniu Tu.Reakcje adaptacyjne wyzwalane i regulowane są przez tyreotropinę, której poziom wzrasta wraz ze wzrostem niedobór jodu. Jeśli dzienne spożycie jodu w organizmie przez długi czas jest mniejsze niż 20 mikrogramów, wówczas długotrwała stymulacja komórek tarczycy prowadzi do rozrostu jej tkanki i rozwoju wola.
Mechanizmy samoregulacyjne gruczołu w warunkach niedoboru jodu zapewniają jego większe wychwytywanie przez tyreocyty przy niższym poziomie jodu we krwi i efektywniejszy recykling. Jeżeli dziennie do organizmu dostarczane jest około 50 mcg jodu, to poprzez zwiększenie szybkości jego wchłaniania przez tyreocyty z krwi (jod pochodzenia spożywczego i jod nadający się do ponownego wykorzystania z produktów przemiany materii), około 100 mcg jodu dziennie dostaje się do tarczycy gruczoł.
Przyjęcie 50 mikrogramów jodu na dobę z przewodu pokarmowego stanowi próg, przy którym długoterminowa zdolność tarczycy do jego akumulacji (w tym jodu ponownie wykorzystanego) w ilościach, gdy zawartość nieorganicznego jodu w gruczole utrzymuje się na najniższym poziomie granica normy (około 10 mg) jest nadal zachowana. Poniżej tego progu dziennego spożycia jodu przez organizm skuteczność zwiększonego tempa pobierania jodu przez tarczycę jest niewystarczająca, zmniejsza się wchłanianie jodu i jego zawartość w gruczole. W takich przypadkach rozwój dysfunkcji tarczycy staje się bardziej prawdopodobny.
Równocześnie z włączeniem mechanizmów adaptacyjnych tarczycy w przypadku niedoboru jodu obserwuje się zmniejszenie jego wydalania z organizmu z moczem. Dzięki temu adaptacyjne mechanizmy wydalnicze zapewniają wydalanie jodu z organizmu w ciągu doby w ilościach odpowiadających jego niższemu dziennemu pobraniu z przewodu pokarmowego.
Przyjmowanie podprogowych stężeń jodu (poniżej 50 mcg dziennie) prowadzi do zwiększenia wydzielania TSH i jego stymulującego działania na tarczycę. Towarzyszy temu przyspieszenie jodowania reszt tyrozylowych tyreoglobuliny, wzrost zawartości monojodotyrozyn (MIT) i spadek dijodotyrozyny (DIT). Zwiększa się stosunek MIT/DIT, w wyniku czego synteza T 4 maleje, a synteza T 3 wzrasta. Stosunek T3/T4 wzrasta w gruczole i krwi.
W przypadku ciężkiego niedoboru jodu następuje spadek poziomu T4 w surowicy, wzrost poziomu TSH i prawidłowa lub podwyższona zawartość T3. Mechanizmy tych zmian nie są jasno poznane, ale najprawdopodobniej jest to wynikiem wzrostu szybkości tworzenia i wydzielania T 3 , wzrostu stosunku T 3 T 4 oraz wzrostu konwersji T 4 do T3 w tkankach obwodowych.
Zwiększenie tworzenia T 3 w stanach niedoboru jodu jest uzasadnione z punktu widzenia osiągnięcia największych końcowych efektów metabolicznych TG przy najmniejszej z ich pojemności „jodowej”. Wiadomo, że wpływ na metabolizm T 3 jest około 3-8 razy silniejszy niż T 4, ale ponieważ T 3 zawiera w swojej strukturze tylko 3 atomy jodu (a nie 4 jak T 4), to do syntezy jednego Cząsteczka T3 wymaga jedynie 75% kosztów jodu w porównaniu z syntezą T4.
Przy bardzo znacznym niedoborze jodu i pogorszeniu czynności tarczycy na tle wysokiego poziomu TSH zmniejszają się poziomy T 4 i T 3. W surowicy krwi pojawia się więcej tyreoglobuliny, której poziom koreluje z poziomem TSH.
Niedobór jodu u dzieci w większym stopniu niż u dorosłych wpływa na procesy metaboliczne w tyreocytach tarczycy. W obszarach zamieszkania dotkniętych niedoborem jodu zaburzenia czynności tarczycy u noworodków i dzieci występują znacznie częściej i są bardziej nasilone niż u dorosłych.
Gdy do organizmu człowieka dostanie się niewielki nadmiar jodu, wzrasta stopień organizacji jodku, synteza trójglicerydów i ich wydzielanie. Występuje wzrost poziomu TSH, nieznaczny spadek poziomu wolnego T 4 w surowicy, przy jednoczesnym zwiększeniu w niej zawartości tyreoglobuliny. Dłuższe nadmierne spożycie jodu może blokować syntezę TG poprzez hamowanie aktywności enzymów biorących udział w procesach biosyntezy. Pod koniec pierwszego miesiąca obserwuje się wzrost wielkości tarczycy. Przy chronicznym nadmiernym przyjmowaniu nadmiaru jodu w organizmie może rozwinąć się niedoczynność tarczycy, jednak jeśli spożycie jodu w organizmie powróci do normy, wówczas wielkość i funkcja tarczycy mogą powrócić do pierwotnych wartości.
Źródłami jodu, które mogą powodować nadmierne spożycie jodu, są często sól jodowana, złożone preparaty multiwitaminowe zawierające suplementy mineralne, żywność i niektóre leki zawierające jod.
Tarczyca posiada wewnętrzny mechanizm regulacyjny, który pozwala skutecznie radzić sobie z nadmiarem jodu. Chociaż spożycie jodu w organizmie może się zmieniać, stężenie TG i TSH w surowicy krwi może pozostać niezmienione.
Uważa się, że maksymalna ilość jod, który przyjęty do organizmu nie powoduje jeszcze zmian w pracy tarczycy, wynosi dla dorosłych około 500 mcg dziennie, jednak następuje wzrost poziomu wydzielania TSH w odpowiedzi na działanie leków uwalniających tyreotropinę hormon.
Spożycie jodu w ilości 1,5-4,5 mg dziennie prowadzi do znacznego obniżenia w surowicy poziomu T 4 całkowitego i wolnego, wzrostu poziomu TSH (poziom T 3 pozostaje niezmieniony).
Efekt nadmiernego jodu hamującego czynność tarczycy występuje także w tyreotoksykozie, gdy przyjęcie jodu w nadmiernej ilości (w stosunku do naturalnego dobowego zapotrzebowania) powoduje eliminację objawów tyreotoksykozy i obniżenie poziomu trójglicerydów w surowicy. Jednak przy długotrwałym przyjmowaniu nadmiaru jodu do organizmu objawy tyreotoksykozy powracają. Uważa się, że przejściowy spadek poziomu TG we krwi przy nadmiernym spożyciu jodu wynika przede wszystkim z hamowania wydzielania hormonów.
Spożycie małych nadmiarowe ilości jod powoduje proporcjonalne zwiększenie jego wychwytu przez tarczycę, aż do określonej wartości nasycenia wchłoniętego jodu. Po osiągnięciu tej wartości pobieranie jodu przez gruczoł może się zmniejszyć pomimo jego spożycia przez organizm w dużych ilościach. W tych warunkach, pod wpływem przysadkowego TSH, aktywność tarczycy może się znacznie różnić.
Ponieważ poziom TSH wzrasta, gdy nadmiar jodu dostanie się do organizmu, można spodziewać się nie początkowego tłumienia, ale aktywacji funkcji tarczycy. Ustalono jednak, że jod hamuje wzrost aktywności cyklazy adenylanowej, hamuje syntezę tyreoperoksydazy, hamuje powstawanie nadtlenku wodoru w odpowiedzi na działanie TSH, chociaż wiązanie TSH z receptorem błony komórkowej tyreocytów jest nie przeszkadza.
Zauważono już, że tłumienie funkcji tarczycy przez nadmiar jodu jest tymczasowy i wkrótce funkcja zostaje przywrócona pomimo ciągłego przyjmowania nadmiernych ilości jodu w organizmie. Następuje adaptacja lub ucieczka tarczycy przed wpływem jodu. Jednym z głównych mechanizmów tej adaptacji jest zmniejszenie efektywności pobierania i transportu jodu do tyreocytów. Ponieważ uważa się, że transport jodu przez błonę podstawną tyreocytów jest związany z funkcją ATPazy Na+/K+, można spodziewać się, że nadmiar jodu może wpływać na jego właściwości.
Pomimo istnienia mechanizmów adaptacji tarczycy do niewystarczającego lub nadmiernego spożycia jodu w celu jego utrzymania normalna funkcja Należy utrzymać równowagę jodu w organizmie. Przy normalnym poziomie jodu w glebie i wodzie na dobę do 500 μg jodu w postaci jodku lub jodanu, które w żołądku przekształcają się w jodki, może przedostać się do organizmu człowieka wraz z pokarmami roślinnymi i w mniejszym stopniu , z wodą. Jodki są szybko wchłaniane z przewodu pokarmowego i rozprowadzane do płynu pozakomórkowego organizmu. Stężenie jodku w przestrzeniach pozakomórkowych pozostaje niskie, ponieważ część jodku jest szybko wychwytywana z płynu pozakomórkowego przez tarczycę, a reszta jest wydalana z organizmu w nocy. Szybkość wychwytu jodu przez tarczycę jest odwrotnie proporcjonalna do szybkości jego wydalania przez nerki. Jod może być wydalany przez ślinę i inne gruczoły przewodu pokarmowego, ale następnie jest ponownie wchłaniany z jelit do krwi. Wydalane jest około 1-2% jodu gruczoły potowe, i kiedy zwiększone pocenie się proporcja jodu wydalanego z jodem może osiągnąć 10%.
Z 500 μg jodu wchłoniętego z jelita górnego do krwi, około 115 μg jest wychwytywane przez tarczycę, a około 75 μg jodu dziennie zużywane jest na syntezę trójglicerydów, 40 μg wraca z powrotem do płynu pozakomórkowego . Zsyntetyzowane T 4 i T 3 ulegają następnie rozkładowi w wątrobie i innych tkankach, uwolniony jod w ilości 60 µg przedostaje się do krwi i płynu zewnątrzkomórkowego, a około 15 µg jodu sprzężonego w wątrobie z glukuronidami lub siarczanami jest wydalane z żółć.
W całkowitej objętości krew jest płynem zewnątrzkomórkowym, który u osoby dorosłej stanowi około 35% masy ciała (czyli około 25 litrów), w którym rozpuszczonych jest około 150 mikrogramów jodu. Jodek jest swobodnie filtrowany w kłębuszkach i około 70% biernie wchłaniany w kanalikach. W ciągu dnia około 485 mikrogramów jodu jest wydalane z organizmu z moczem i około 15 mikrogramów z kałem. Średnie stężenie jodu w osoczu krwi utrzymuje się na poziomie około 0,3 µg/l.
Wraz ze spadkiem spożycia jodu w organizmie zmniejsza się jego ilość w płynach ustrojowych, zmniejsza się wydalanie z moczem, a tarczyca może zwiększyć jego wchłanianie o 80-90%. Tarczyca jest w stanie magazynować jod w postaci jodotyroniny i jodowanej tyrozyny w ilościach zbliżonych do 100-dniowego zapotrzebowania organizmu. Dzięki mechanizmom oszczędzającym jod i odkładaniu się jodu, synteza TG w warunkach niedoboru jodu w organizmie może pozostać niezakłócona nawet przez dwa miesiące. Dłuższy niedobór jodu w organizmie prowadzi do zmniejszenia syntezy trójglicerydów pomimo jego maksymalnego pobrania przez gruczoł z krwi. Zwiększenie spożycia jodu w organizmie może przyspieszyć syntezę trójglicerydów. Jeśli jednak dzienne spożycie jodu przekracza 2000 mcg, gromadzenie się jodu w tarczycy osiąga poziom, przy którym wychwyt jodu i biosynteza hormonów są zahamowane. Przewlekłe zatrucie jodem ma miejsce, gdy jego dzienne spożycie w organizmie przekracza 20-krotność dziennego zapotrzebowania.
Jodek dostający się do organizmu jest z niego wydalany głównie z moczem, dlatego jego całkowita zawartość w objętości dobowego moczu jest najdokładniejszym wskaźnikiem spożycia jodu i może służyć do oceny bilansu jodowego w całym organizmie.
Zatem do syntezy trójglicerydów w ilościach adekwatnych do potrzeb organizmu niezbędna jest wystarczająca podaż egzogennego jodu. Jednocześnie normalna realizacja działania TG zależy od skuteczności ich wiązania z receptorami jądrowymi komórek, do których zalicza się cynk. Dlatego też spożycie wystarczającej ilości tego mikroelementu (15 mg/dzień) jest istotne także dla uzewnętrznienia działania TH na poziomie jądra komórkowego.
Tworzenie aktywnych form TH z tyroksyny w tkankach obwodowych następuje pod wpływem dejodynaz, obecność selenu jest niezbędna do przejawu ich działania. Ustalono, że spożycie selenu w organizmie osoby dorosłej w ilości 55-70 µg na dobę jest warunkiem niezbędnym do wytworzenia wystarczającej ilości Tv w tkankach obwodowych.
Nerwowe mechanizmy regulacji funkcji tarczycy realizowane są poprzez wpływ neuroprzekaźników ATP i PSNS. SNS unerwia naczynia gruczołu i tkankę gruczołową za pomocą włókien pozazwojowych. Norepinefryna zwiększa poziom cAMP w tyreocytach, nasila wchłanianie przez nie jodu, syntezę i wydzielanie hormonów tarczycy. Włókna PSNS nadają się również do budowy pęcherzyków i naczyń tarczycy. Zwiększeniu napięcia PSNS (lub wprowadzeniu acetylocholiny) towarzyszy wzrost poziomu cGMP w tyreocytach i zmniejszenie wydzielania hormonów tarczycy.
Pod kontrolą ośrodkowego układu nerwowego następuje powstawanie i wydzielanie TRH przez neurony drobnokomórkowe podwzgórza, a co za tym idzie wydzielanie TSH i hormonów tarczycy.
Poziom hormonów tarczycy w komórkach tkanek, ich przemiana w formy aktywne i metabolity jest regulowana przez system dejodynaz – enzymów, których działanie zależy od obecności selenocysteiny w komórkach i spożycia selenu. Wyróżnia się trzy rodzaje dejodynaz (D1, D2, DZ), które są w różny sposób rozmieszczone w różnych tkankach organizmu i wyznaczają ścieżki przemiany tyroksyny w aktywny T3 lub nieaktywny pT3 i inne metabolity.
Endokrynologiczna funkcja komórek K przypęcherzykowych tarczycy
Komórki te syntetyzują i wydzielają hormon kalcytoninę.
Kalcytonip (tyrokalcytoina)- peptyd składający się z 32 reszt aminokwasowych, zawartość we krwi wynosi 5-28 pmol/l, działa na komórki docelowe, stymulując receptory błonowe T-TMS i zwiększając w nich poziom cAMP i IGF. Może być syntetyzowany w grasicy, płucach, ośrodkowym układzie nerwowym i innych narządach. Rola kalcytoniny pozatarczycowej jest nieznana.
Fizjologiczną rolą kalcytoniny jest regulacja poziomu wapnia (Ca 2+) i fosforanów (PO 3 4 -) we krwi. Funkcja jest realizowana poprzez kilka mechanizmów:
- hamowanie czynności funkcjonalnej osteoklastów i hamowanie resorpcji kości. Zmniejsza to wydalanie jonów Ca 2+ i PO 3 4 - z tkanki kostnej do krwi;
- zmniejszenie wchłaniania zwrotnego jonów Ca 2+ i PO 3 4 - z moczu pierwotnego w kanalikach nerkowych.
Z powodu tych efektów wzrost poziomu kalcytoniny prowadzi do zmniejszenia zawartości jonów Ca 2 i PO 3 4 we krwi.
Regulacja wydzielania kalcytoniny przeprowadzane przy bezpośrednim udziale Ca 2 we krwi, którego stężenie wynosi zwykle 2,25-2,75 mmol / l (9-11 mg%). Wzrost poziomu wapnia we krwi (hipskalcyzm) powoduje aktywne wydzielanie kalcytoniny. Spadek poziomu wapnia prowadzi do zmniejszenia wydzielania hormonów. Pobudzają wydzielanie kalcytoniny, katecholamin, glukagonu, gastryny i cholecystokininy.
Wzrost poziomu kalcytoniny (50-5000 razy wyższy niż normalnie) obserwuje się w jednej z postaci raka tarczycy (raka rdzeniastego), który rozwija się z komórek parafolikularnych. Jednocześnie oznaczenie wysokiego poziomu kalcytoniny we krwi jest jednym z markerów tej choroby.
Wzrost poziomu kalcytoniny we krwi, a także praktycznie całkowita nieobecność kalcytoninie po usunięciu tarczycy nie może towarzyszyć naruszenie metabolizmu wapnia i układ szkieletowy. Te obserwacje kliniczne sugerują, że fizjologiczna rola kalcytoniny w regulacji poziomu wapnia pozostaje słabo poznana.
Tarczyca(glandula tarczycy) to gruczoł wydzielania wewnętrznego, który syntetyzuje szereg hormonów niezbędnych do utrzymania homeostazy.Tarczyca składa się z dwóch płatów i przesmyku. Płaty sąsiadują z lewą i prawą stroną tchawicy, przesmyk znajduje się na przedniej powierzchni tchawicy. Czasami od przesmyku lub częściej od lewego (rzadziej prawego) płata gruczołu wystaje dodatkowy płat piramidowy. Zwykle masa tarczycy wynosi od 20 do 60 g, wielkość płatów waha się w granicach 5-8'2-4'1-3 cm.
W okresie dojrzewania zwiększa się masa tarczycy podeszły wiek maleje. Kobiety mają większą tarczycę niż mężczyźni; w czasie ciąży następuje jego fizjologiczny wzrost, który znika samoistnie w ciągu 6-12 miesięcy.
po porodzie.
Tarczyca ma zewnętrzną i wewnętrzną torebkę tkanki łącznej. Dzięki torebce zewnętrznej tworzy się aparat więzadłowy, który mocuje gruczoł do tchawicy i krtani (ryc.). Górną granicę gruczołu (płatki boczne) stanowi chrząstka tarczowata, dolna - 5-6 pierścieni tchawiczych. Przesmyk znajduje się na poziomie chrząstek I-III lub II-IV tchawicy.
Tarczyca jest jednym z najbardziej unaczynionych narządów z rozwiniętymi tętnicami i silniejszymi układami żylnymi. Krew wpływa do gruczołu przez dwie tętnice tarczowe górne (odgałęzienia tętnicy szyjnej zewnętrznej) i dwie tętnice tarczowe dolne, które tworzą między sobą zespolenia. Żylne i system limfatyczny przeprowadzają odpływ z tarczycy krwi i limfy zawierającej hormony tarczycy, tyreoglobulinę, a w stanach patologicznych przeciwciała przeciwtarczycowe, immunoglobuliny stymulujące i blokujące tarczycę.
Unerwienie tarczycy odbywa się za pomocą gałęzi nerwu błędnego (przywspółczulnego) i gałęzi zwojów szyjnych (współczulnych).
Główną jednostką strukturalną i funkcjonalną tarczycy są pęcherzyki - pęcherzyki o różnych kształtach, często zaokrąglone, o średnicy 25-500 mikronów, oddzielone od siebie cienkimi warstwami luźnej tkanki łącznej z dużą liczbą naczyń włosowatych krwi i limfy .
Ich światło wypełnione jest koloidem – bezstrukturalną masą zawierającą tyreoglobulinę, która jest syntetyzowana przez pęcherzyki, czyli tak zwane komórki A tworzące ścianę pęcherzyka. Są to komórki nabłonkowe o kształcie sześciennym lub cylindrycznym (ze wzrostem aktywności funkcjonalnej). Wraz ze spadkiem czynności tarczycy spłaszczają się. Wraz z pęcherzykami w tarczycy znajdują się międzypęcherzykowe wyspy komórek nabłonkowych (komórki B, komórki Ascanazi), które są źródłem powstawania nowych pęcherzyków.
Komórki Ascanazi są większe niż komórki A, mają zozynofilową cytoplazmę i zaokrąglone, centralnie położone jądro: aminy biogenne, m.in. serotonina. Oprócz komórek A i B tarczyca zawiera także komórki parafolikularne (komórki C). Znajdują się na zewnętrznej powierzchni mieszków włosowych, są komórkami neuroendokrynnymi, nie wchłaniają jodu i należą do układu APUD.
Tarczyca wydziela dwa hormony zawierające jod, tyroksynę (T4) i trójjodotyroninę (T3) oraz jeden hormon peptydowy, kalcytoninę.
Tyroksyna i trójjodotyronina są syntetyzowane w wierzchołkowej części nabłonka tarczycy i częściowo w przestrzeni wewnątrzpęcherzykowej, gdzie kumulują się i stają się częścią tyreoglobuliny. Kalcytonina (tyreokalcytonina) jest wytwarzana przez komórki C tarczycy, a także przytarczyce i grasicę.
Komórki pęcherzykowe tarczycy posiadają wyjątkową zdolność wychwytywania jodu z krwiobiegu, który przy udziale hodowcy peroksydazy wiąże się z tyreoglobuliną koloidalną. Tyreoglobulina pełni rolę wewnątrzpęcherzykowej rezerwy hormonów tarczycy. W razie potrzeby, poprzez pinocytozę, pewna jej ilość przedostaje się do komórki pęcherzykowej, gdzie w wyniku proteolizy T3 i T4 są uwalniane z tyreoglobuliny i oddzielane od innych hormonalnie nieaktywnych jodowanych peptydów.
Wolne hormony dostają się do krwi, a białka jodu ulegają dejodyzacji; Uwolniony jod wykorzystywany jest do syntezy nowych hormonów tarczycy. Szybkość rozkładu tyreoglobuliny, synteza hormonów tarczycy zależy zarówno od regulacji ośrodkowej, jak i od poziomu jodu i krwi oraz obecności w niej substancji wpływających na metabolizm jodu (globuliny immunostymulujące, tiocyjaniany, bromki itp.). Tym samym ich synteza i wydzielanie przebiega z taką szybkością i taką ilością, że organizm musi utrzymać stężenie hormonów w tkankach zapewniających homeostazę. To ostatnie osiąga się poprzez złożony system regulacji centralnej i peryferyjnej.
Regulacja centralna odbywa się poprzez wytwarzanie tyroliberyny (czynnika uwalniającego hormon tyreotropowy) i ewentualnie tyreostatyny (czynnik hamujący syntezę hormonu tyreotropowego). Hormon tyreotropowy (TSH) syntetyzowany przez tyreotrofy przedniego płata przysadki mózgowej, stymuluje wzrost i aktywność funkcjonalną nabłonka tarczycy.
Wejście TSH do krwi regulowane jest przez poziom stężenia hormonów tarczycy we krwi i tyreoliberyny, jednak głównym czynnikiem regulacyjnym jest stężenie hormonów tarczycy we krwi; wyjątkowo wysoki poziom tego ostatniego powoduje, że tyreotrofy są oporne na tyreoliberynę.
Obwodowa regulacja metabolizmu tarczycy zależy od liczby specyficznych receptorów dla hormonów tarczycy w komórce; w warunkach wysoka zawartość hormony tarczycy, ich liczba jest zmniejszona, przy niskiej zawartości - wzrasta. Ponadto większość tyroksyny może zostać metabolizowana do postaci nieaktywnej i w ten sposób realizować jeden z rodzajów obwodowej regulacji stanu funkcjonalnego organizmu.
Fizjologiczna zawartość hormonów tarczycy jest niezbędna do prawidłowej syntezy białek w różne ciała i tkanki (od centralnego układu nerwowego po tkankę kostną); ich nadmiar prowadzi do rozłączenia oddychania tkankowego i fosforylacji oksydacyjnej w mitochondriach komórkowych, a następnie gwałtownego zmniejszenia rezerw energetycznych organizmu.
Ponadto, zwiększając wrażliwość receptorów na katecholaminy, hormony tarczycy powodują zwiększoną pobudliwość autonomicznego układu nerwowego, objawiającą się tachykardią, arytmią, podwyższonym skurczowym ciśnieniem krwi, wzmożoną motoryką przewodu pokarmowego i wydzielaniem soków trawiennych: zwiększają także rozkład glikogenu, hamują jego syntezę w wątrobie, wpływają metabolizm lipidów. Brak hormonów tarczycy powoduje gwałtowne zmniejszenie tempa wszelkich procesów oksydacyjnych w organizmie i gromadzenie się glikozaminoglikanów. Najbardziej wrażliwe na te zmiany są komórki centralnego układu nerwowego. mięsień sercowy, gruczoły wydzielania wewnętrznego.
METODY BADAWCZE
Badanie pacjentów z patologią tarczycy obejmuje kliniczne, laboratoryjne metody oceny jej aktywności funkcjonalnej, a także metody dożylnego (przedoperacyjnego) badania struktury gruczołu. Palpacja tarczycy określa jej wielkość, konsystencję oraz obecność lub brak formacji guzkowych. Najbardziej pouczające metody laboratoryjne oznaczanie hormonów tarczycy we krwi to metody radioimmunologiczne przeprowadzane przy użyciu standardowych zestawów testowych.
O stanie funkcjonalnym tarczycy decyduje wchłanianie nadtechnecjanu 131I lub 99mTc. Do metod oceny budowy tarczycy in vivo zalicza się tomografię komputerową, diagnostykę ultrasonograficzną, skanowanie radionuklidów i scyntygrafię, które dostarczają informacji o topografii, wielkości i charakterze nagromadzenia radiofarmaceutyku w różnych częściach gruczołu, a także biopsja punkcyjna (aspiracyjna), a następnie mikroskopia punktowa.
PATOLOGIA
Objawy kliniczne chorób tarczycy są spowodowane albo nadmierną lub niedostateczną produkcją hormonów tarczycy, albo nadmierną produkcją kalcytoniny i prostaglandyn (na przykład w raku rdzeniastym - guz wytwarzający kalcytoninę), a także objawami ucisku tkanek i narządy szyi powiększonej tarczycy bez upośledzonej produkcji hormonów (eutyreoza).
Wyróżnia się pięć stopni powiększenia tarczycy: stopień O – gruczoł nie jest widoczny w badaniu i nie można go określić palpacyjnie; I stopień - podczas połykania widoczny jest przesmyk, który określa się palpacją lub dotyka się jednego z płatów tarczycy i przesmyku; II stopień - obmacuje się oba płaty, ale podczas badania kontury szyi nie ulegają zmianie; III stopień – tarczyca jest powiększona zarówno w obrębie płatów, jak i cieśni, widoczna na pierwszy rzut oka jako zgrubienie na przedniej powierzchni szyi (szyja gruba); Stopień IV - wole duże, niezbyt asymetryczne, z oznakami ucisku pobliskich tkanek i narządów szyi; Stopień V - wole o wyjątkowo dużych rozmiarach.
Wady rozwojowe. Aplazja (brak) tarczycy jest rzadka z powodu naruszenia różnicowania embrionalnego zarodka tkanki tarczycy: wykrywa się ją we wczesnym dzieciństwie na podstawie obrazu klinicznego ciężkiej wrodzonej niedoczynności tarczycy.
Wrodzona hipoplazja tarczycy rozwija się z powodu braku jodu w organizmie matki, klinicznie objawiającego się kretynizmem i opóźnieniem w rozwoju fizycznym dziecka. Głównym rodzajem leczenia obu stanów patologicznych jest dożywotnia hormonalna terapia zastępcza.
Przy zachowaniu przewodu tarczowo-językowego często tworzą się środkowe torbiele i przetoki szyi, a także wole korzenia języka, które należy usunąć. Przemieszczenie podstaw tarczycy do śródpiersia prowadzi do rozwoju wola zamostkowego lub guza. Źródłem ich powstawania mogą być także ogniska dystopii tkanki tarczycy w ścianie tchawicy, gardła, mięśnia sercowego, osierdzia.
Urazy tarczycy są niezwykle rzadkie, zwykle łączą się z urazami innych narządów szyi. Z reguły otwartym zmianom towarzyszą obfite krwawienie wymagają pilnej opieki chirurgicznej. Zamknięte urazy obserwuje się, gdy szyja jest ściśnięta (na przykład pętla podczas próby samobójczej), objawiająca się powstaniem krwiaka.
CHOROBY
Wśród chorób tarczycy najczęstszym wolem jest rozsiane toksyczne i autoimmunologiczne zapalenie tarczycy, które uważane jest za typowe choroby autoimmunologiczne o podobnej patogenezie, ale innym obrazie klinicznym, często spotykane u krewnych. Grupa zaraźliwa choroby zapalne Tarczyca łączy stany patologiczne o różnych objawach klinicznych, charakteryzujące się wspólnymi objawami związanymi z uciskiem tkanek i narządów otaczających tarczycę.
Guzy. Charakterystycznymi łagodnymi guzami nabłonkowymi tarczycy są gruczolaki o różnej budowie histologicznej. Kliniczne wykrywanie gruczolaków opiera się na badaniu palpacyjnym guza tarczycy o wyraźnych konturach i gładkiej powierzchni, który z czasem powoli powiększa się.
Węzły chłonne szyjne nienaruszone, funkcja gruczołów najczęściej nie ulega zmianie. W warunkach ambulatoryjnych w rozpoznaniu łagodne nowotwory oprócz palpacji ważną rolę odgrywa badanie tarczycy, badanie ultrasonograficzne, a następnie badanie cytologiczne punktu punkcikowego. Podstawową zasadą chirurgii wątroby jest usunięcie płata gruczołu, w którym zlokalizowany jest guz (hemityreoidektomia). Rokowanie po leczeniu chirurgicznym gruczolaków jest korzystne.
Najczęstsze są nowotwory złośliwe tarczycy różne formy raka i stanowią 0,5–2,2% wszystkich nowotworów złośliwych. Inne rodzaje raka tarczycy są mniej powszechne. Do chorób przednowotworowych zalicza się wole guzkowe i mieszane, a także gruczolaki tarczycy.
Rozwojowi raka tarczycy sprzyja wysokie wydzielanie hormonu tyreotropowego przez przysadkę mózgową (obserwowane częściej u osób żyjących w endemicznych strefach wola) oraz prześwietlenie lub inne napromienianie głowy i szyi, górnego śródpiersia, przeprowadzane w celach diagnostycznych i (lub) terapeutycznych u dzieci i młodzieży. Szczególne znaczenie w rozwoju raka tarczycy ma połączenie ekspozycja zewnętrzna określone obszary z wewnętrznym narażeniem na włączone radionuklidy jodu w przypadku skażenia środowisko substancje radioaktywne.
Klinicznie rak tarczycy objawia się zwykle na dwa sposoby. Częściej guz tarczycy i obecność (lub brak) regionalnych (węzłów chłonnych przednio-bocznych odcinków szyi, okolic nadobojczykowych i podobojczykowych, a także przedniego górnego śródpiersia) i odległych (płuca, kości itp. .) określa się przerzuty. Podczas badania palpacyjnego gruczołu stwierdza się gęsty, wyboisty, często słabo przemieszczony guz, który z czasem prowadzi do zmiany głosu, zaburzeń oddychania lub połykania.
W drugim wariancie klinicznym guz ze względu na niewielkie rozmiary nie jest wykrywany palpacyjnie, a także metodami radionuklidowymi i ultradźwiękowymi („ukryty rak” tarczycy); na pierwszy plan wysuwają się przerzuty w regionalnych węzłach chłonnych i (lub) w narządach odległych. Szczególnie wyróżnia się tzw. wysoko zróżnicowany rak pęcherzykowy (gruczolak złośliwy, przerzutowy struma Langhansa, gruczolak angioinwazyjny), który przy stosunkowo dojrzałej strukturze charakteryzuje się inwazyjnym wzrostem i zdolnością do przerzutów.
Rozpoznanie raka tarczycy jest bardzo trudne w przypadku obecności długotrwałego wola lub gruczolaka, których wiodącymi objawami złośliwości są ich szybki wzrost, zagęszczenie, pojawienie się guzowatości, a następnie ograniczenie przemieszczenia gruczołu. Ostateczną diagnozę ustala się jedynie na podstawie badania cytologicznego lub badanie histologiczne.
W przypadku „raka ukrytego” wraz z oznaczeniem poziomu kalcytoniny (rak rdzeniasty) końcowym etapem diagnozy jest często szerokie naświetlenie i rewizja tarczycy. Diagnostyka różnicowa guzów tarczycy opiera się na danych klinicznych i radiologicznych, wynikach badania gruczołu, USG i tomografii komputerowej, celowanym nakłuciu guza i późniejszym badaniu cytologicznym punkcika.
Leczenie chirurgiczne obejmuje hemityreoidektomię, subtotalną resekcję tarczycy i tyroidektomię. W przypadku obecności regionalnych przerzutów na szyi wykonuje się wycięcie powięziowo-pochewkowe tkanki szyi. W przypadku obecności przerzutów odległych nowotworu miejscowo operacyjnego wskazane jest wycięcie tarczycy, a następnie leczenie jodem radioaktywnym.
Rokowanie jest korzystne w przypadku zróżnicowanych postaci nowotworu (pęcherzykowego i brodawkowatego), a niekorzystne w przypadku pozostałych postaci. Profilaktyka raka tarczycy ma na celu przede wszystkim leczenie wola i nowotworów łagodnych, wykluczenie ekspozycji na promieniowanie rentgenowskie oraz radioterapia obszar tarczycy u dzieci i młodzieży, zapobiegając przedostawaniu się radionuklidów jodu do organizmu z pożywieniem i wodą.
We wczesnym wykrywaniu raka tarczycy dużą rolę odgrywa badanie kliniczne pacjentów z różnymi postaciami wola i ich leczenie chirurgiczne, a także badanie krewnych pacjentów cierpiących na tę chorobę rak rdzeniasty tarczycy, szczególnie w przypadkach zespołu Sipple’a i zespołu nerwiaka błony śluzowej w połączeniu z gruczolakowatością gruczołów dokrewnych.
Operacje na tarczycy wykonuje się jak poniżej znieczulenie miejscowe i w znieczuleniu intubacyjnym. Pacjenci z tyreotoksykozą przed operacją wymagają specjalnego przygotowania przedoperacyjnego. Najwygodniejszym dostępem do tarczycy jest łukowe nacięcie poprzeczne na przedniej powierzchni szyi, 1–1,5 cm powyżej wcięcia szyjnego. W większości przypadków zamostkowe postacie wola można również usunąć za pomocą tego dostępu, chociaż czasami konieczne jest zastosowanie, podobnie jak u pacjentów z wolem wewnątrzklatkowym, torakotomii.
Cechą charakterystyczną każdej operacji tarczycy jest zakres interwencji oraz sposób (metoda) usunięcia tkanki tarczycy. Wyróżnia się metody wewnątrztorebkowe, dopowięziowe i zewnątrzpowięziowe. Metoda wewnątrztorebkowa jest zwykle stosowana do wyłuszczenia guzków tarczycy w celu maksymalnego zachowania niezmienionej tkanki gruczołu.
We wszystkich postaciach wola stosuje się śródpowięziową izolację tarczycy, przy czym nie dochodzi do urazu gałęzi nerwu krtaniowego wstecznego, a przytarczyce zostają zachowane, zlokalizowane na zewnątrz (rzadziej wewnątrz) płata trzewnego powięzi IV. szyi, w obrębie której wykonywana jest operacja. Czasami tę metodę uzupełnia się podwiązaniem tętnic na całej długości. Metodę zewnątrzpowięziową przeprowadza się wyłącznie w praktyka onkologiczna i z reguły wiąże się z ubieraniem główne arterie Tarczyca.
Objętość interwencji chirurgicznej zależy od charakteru i lokalizacji procesu patologicznego, wielkości ogniska patologicznego i ilości pozostałej tkanki. Najczęściej stosowana jest częściowa, subtotalna resekcja i wytępienie (całkowite usunięcie) jednego lub obu płatów tarczycy. Częściowa resekcja stosuje się go w przypadku małych wola guzowatych, łagodnych, przy zachowaniu około połowy usuniętego płata (płatków).
Resekcja częściowa polega na pozostawieniu od 4 do 8 g tkanki gruczołowej w każdym płacie (zwykle na bocznej powierzchni tchawicy, w okolicy nerwów krtaniowych wstecznych i przytarczyc). Taką interwencję wykonuje się w przypadku wszystkich postaci wola u pacjentów z tyreotoksykozą, a także wola guzkowego i wieloguzkowego eutyreozy, które zajmują prawie cały płat (płatki) tarczycy.
Wytępienie stosuje się z reguły w przypadku nowotworów złośliwych tarczycy, operację tę można uzupełnić, w zależności od stadium i lokalizacji procesu, poprzez usunięcie mięśni przylegających do gruczołu, żył szyjnych zewnętrznych i wewnętrznych z tkanką zawierającą węzły chłonne.
Wśród możliwych powikłań występujących po operacji tarczycy należy wymienić niedowład nerwów krtaniowych wstecznych i niedoczynność przytarczyc, a także wtórne krwawienia we wczesnym okresie pooperacyjnym.
Tarczyca (gruczoł tarczycy) jest nieparzystym narządem zlokalizowanym w przedniej części szyi, na poziomie krtani i górnej tchawicy. Gruczoł składa się z dwóch płatów - prawego (lobus zwinny) i lewego (lobus sinister), połączonych wąskim przesmykiem. Tarczyca leży raczej powierzchownie. Przed gruczołem, poniżej kości gnykowej, znajdują się pary mięśni: mostkowo-tarczowy, mostkowo-gnykowy, łopatkowo-gnykowy i tylko częściowo mostkowo-obojczykowo-sutkowy, a także powierzchowne i przedtchawicze płytki powięzi szyjnej.
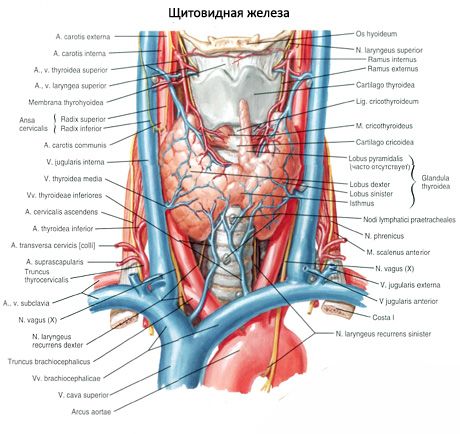

Tylna wklęsła powierzchnia gruczołu pokrywa przód i boki dolnych odcinków krtani i Górna część tchawica. Cieśń tarczycy (isthmus gruczołu tarczycowego), który łączy płat prawy i lewy, zwykle znajduje się na poziomie II lub III chrząstki tchawicy. W rzadkich przypadkach cieśń gruczołu leży na poziomie I chrząstki tchawicy lub nawet łuku chrząstki pierścieniowatej. Czasami przesmyk może być nieobecny, a wtedy płaty gruczołu w ogóle nie są ze sobą połączone.
Górne bieguny prawego i lewego płata tarczycy znajdują się nieco poniżej górnej krawędzi odpowiedniej płytki chrząstki tarczowatej krtani. Dolny biegun płata sięga poziomu chrząstki V-VI tchawicy. Tylno-boczna powierzchnia każdego płata tarczycy styka się z krtaniową częścią gardła, początkiem przełyku i przednim półkolem tętnicy szyjnej wspólnej. Przytarczyce przylegają do tylnej powierzchni prawego i lewego płata tarczycy.
Od cieśni lub od jednego z płatów płat piramidowy (lobus piramidalis) rozciąga się ku górze i znajduje się przed chrząstką tarczowatą, co występuje w około 30% przypadków. Płat ten wraz z wierzchołkiem czasami sięga do trzonu kości gnykowej.
Poprzeczny rozmiar tarczycy u osoby dorosłej sięga 50-60 mm. Rozmiar wzdłużny każdego lemiesza wynosi 50-80 mm. Pionowy rozmiar przesmyku wynosi od 5 do 2,5 mm, a jego grubość wynosi 2-6 mm. Masa tarczycy u dorosłych w wieku od 20 do 60 lat wynosi średnio 16,3-18,5 g. Po 50-55 latach następuje niewielki spadek objętości i masy gruczołu. Masa i objętość tarczycy u kobiet jest większa niż u mężczyzn.
Na zewnątrz tarczyca pokryta jest osłoną tkanki łącznej - kapsułka włóknista(capsula fibrosa), która jest połączona z krtanią i tchawicą. Pod tym względem, gdy krtań się porusza, porusza się również tarczyca. Wewnątrz gruczołu od torebki odchodzą przegrody tkanki łącznej - beleczki, dzieląc tkankę gruczołu na zraziki, które składają się z mieszki włosowe.Ściany pęcherzyków są wyłożone od wewnątrz sześciennymi nabłonkowymi komórkami pęcherzykowymi (tyrocytami), a wewnątrz pęcherzyków znajduje się gęsta substancja – koloid. Koloid zawiera hormony tarczycy, które składają się głównie z białek i aminokwasów zawierających jod.
Ściany każdego pęcherzyka (jest ich około 30 milionów) utworzone są przez pojedynczą warstwę tyreocytów umiejscowionych na błonie podstawnej. Rozmiar mieszków włosowych wynosi 50-500 mikronów. Kształt tyreocytów zależy od aktywności zachodzących w nich procesów syntetycznych. Im bardziej aktywny jest stan funkcjonalny tyreocytu, tym wyższa jest komórka. Tyrocyty mają duże jądro w środku, znaczną liczbę rybosomów, dobrze rozwinięty kompleks Golgiego, lizosomy, mitochondria i granulki wydzielnicze w części wierzchołkowej. Na wierzchołkowej powierzchni tyreocytów znajdują się mikrokosmki zanurzone w koloidie znajdującym się w jamie pęcherzyka.
Gruczołowy nabłonek pęcherzykowy tarczycy, bardziej niż inne tkanki, ma selektywną zdolność do akumulacji jodu. W tkankach tarczycy stężenie jodu jest 300 razy wyższe niż jego zawartość w osoczu krwi. Hormony tarczycy (tyroksyna, trójjodotyronina), będące złożonymi związkami jodowanych aminokwasów z białkiem, mogą gromadzić się w koloidie pęcherzyków i w razie potrzeby być uwalniane do krwioobiegu i dostarczane do narządów i tkanek.
Hormony tarczycy
Hormony tarczycy regulują metabolizm, zwiększają wymianę ciepła, wzmagają procesy oksydacyjne oraz zużycie białek, tłuszczów i węglowodanów, wspomagają uwalnianie wody i potasu z organizmu, regulują procesy wzrostu i rozwoju, aktywują aktywność nadnerczy, płci i piersi gruczoły, działają stymulująco na czynność ośrodkowego układu nerwowego.
Pomiędzy tyreocytami na błonie podstawnej, a także pomiędzy pęcherzykami znajdują się komórki parafolikularne, których wierzchołki sięgają światła pęcherzyka. Komórki parafolikularne mają duże zaokrąglone jądro, dużą liczbę miofilamentów w cytoplazmie, mitochondria, kompleks Golgiego i ziarnistą siateczkę śródplazmatyczną. Komórki te zawierają wiele granulek o dużej gęstości elektronowej i średnicy około 0,15 µm. Komórki parafolikularne syntetyzują tyrokalcytoninę, która jest antagonistą hormonu przytarczyc – hormonu gruczołów przytarczyc. Tyrokalcytonina bierze udział w wymianie wapnia i fosforu, zmniejsza zawartość wapnia we krwi i opóźnia uwalnianie wapnia z kości.
Regulację pracy tarczycy zapewnia układ nerwowy i hormon tyreotropowy przedniego płata przysadki mózgowej.
Embriogeneza tarczycy
Tarczyca rozwija się z nabłonka przedniego jelita w postaci niesparowanego środkowego wyrostka na poziomie między I i II łukiem trzewnym. Do 4 tygodni rozwój zarodkowy ten wyrostek ma jamę, w związku z którą otrzymał nazwę przewodu tarczycowego (przewód tarczycowy). Pod koniec czwartego tygodnia przewód ten zanika, a jego początek pozostaje jedynie w postaci mniej lub bardziej głębokiej ślepej dziury na granicy nasady i trzonu języka. Kanał dystalny jest podzielony na dwie podstawy przyszłych płatów gruczołu. Pojawiające się płaty tarczycy są przemieszczane w kierunku ogonowym i przyjmują swoje zwykłe położenie. Zachowana dystalna część przewodu tarczowo-językowego zamienia się w płat piramidalny narządu. Zmniejszenie odcinków przewodu może służyć jako początek tworzenia dodatkowych gruczołów tarczowych.

Naczynia i nerwy tarczycy
Tętnice tarczowe górne prawe i lewe (odgałęzienia tętnic szyjnych zewnętrznych) dochodzą odpowiednio do biegunów górnych prawego i lewego płata tarczycy, a tętnice tarczowe dolne prawa i lewa (od pni szyjnych tarczycy tętnic podobojczykowych) do dolne bieguny tych płatów. Gałęzie tętnic tarczowych tworzą liczne zespolenia w torebce gruczołu i wewnątrz narządu. Czasami tzw. dolna tętnica tarczowa, która odchodzi od pnia ramienno-głowowego, zbliża się do dolnego bieguna tarczycy. Odtleniona krew z tarczycy przepływa przez żyły tarczowe górne i środkowe do żyły szyjnej wewnętrznej, przez żyłę tarczową dolną do żyły ramienno-głowowej (lub do dolna częśćżyła szyjna wewnętrzna).
Naczynia limfatyczne tarczycy wpływają do węzłów chłonnych tarczycowych, przedkrtaniowych, przedtchawiczych i przytchawiczych. Nerwy tarczycy odchodzą od węzłów szyjnych prawego i lewego pnia współczulnego (głównie od środkowego węzła szyjnego, biegną wzdłuż naczyń), a także od nerwów błędnych.
